(2 上海临床研究中心,上海科技大学,上海 201210)
(2 Shanghai Clinical Research and Trial Center, ShanghaiTech University, Shanghai 201210, China)
质谱(mass spectrometry)是一种将分子离子化并根据其质荷比(m/z)进行分离和检测的分析技术。质谱技术工作流程可分为几个主要步骤:(1)离子化;(2)离子传输;(3)离子碎裂;(4)质量分析;(5)检测。质谱仪通常由以下几个核心部件组成:(1)离子源(主要有电喷雾离子化、基质辅助激光解吸离子化);(2)离子传输和质量分析器(主要有四极杆、飞行时间、离子阱等);(3)检测器(包括电子倍增器、微通道板等);(4)真空系统(机械泵、分子涡轮泵等);(5)电子控制与数据处理系统(控制软件、谱图解析软件等);(6)离子碰撞池(对于复杂分子如蛋白质和多肽,需要将离子进一步碎裂,获得碎片信号,进行结构解析)。分子质量是所有物质固有和特异的属性,只要能将物质离子化,质谱就能对其进行定性,同时质谱对离子的检测是浓度依赖的,提供了定量信息,因此质谱技术对物质的定性和定量能力是无可替代的。
如果回溯质谱技术的发展历史,我们会发现,在物理学的世纪——20世纪,在伟大的1905年,爱因斯坦在瑞士发表了相对论。与此同时,在欧洲海峡对面的英国剑桥卡文迪许实验室,汤姆逊开始研究阳极射线,他发现放电管中的氖在电磁场作用下,会出现两条阳射线抛物线,随后阿斯顿加入卡文迪许实验室,制作了最初的阳离子偏转器,证实了同位素的存在,这是质谱仪的雏形[1],这一起步迄今约120年。在这120年中,科学家们不断激发各种分子成为带电离子,在电磁场中运动,进而被分辨和检测。
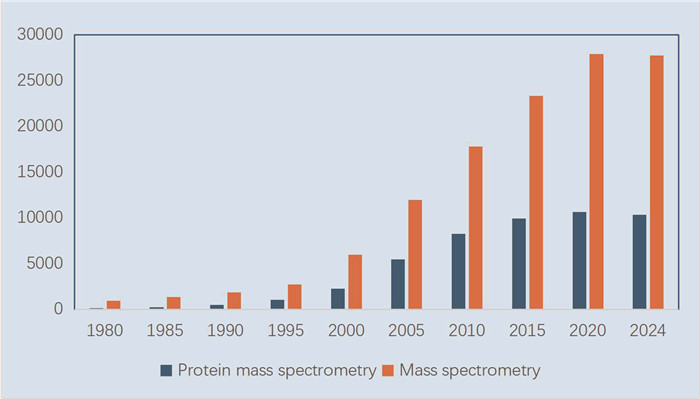
在质谱技术发明后的近80年里,大部分应用是针对小分子的,如今对于无机和有机小分子的应用仍非常广泛,在生命科学中,也独立衍生出代谢组学这一分支。然而,在此起彼伏的技术浪潮中,最令人激动的还是质谱技术应用于生物大分子,尤其是蛋白质。因为蛋白质本身的复杂性和动态性,对技术的分辨率、准确度、覆盖率、灵敏度有不同层次的要求。依据PubMed数据统计,从1980年到2024年,每隔5年以mass spectrometry为关键词查询,检索得到的文章数量从994篇增长到27 732篇;若以protein mass spectrometry查询,文章数量则从113篇增加到10 342篇,无论是增长速度还是占比,蛋白质相关研究都超过其他应用(图 1)。
|
图 1 每隔五年以mass spectrometry和protein mass spectrometry为关键词检索得到的论文数量统计图(1980—2024年)(PubMed) |
可以说,生物质谱技术发展的很多里程碑是以蛋白质研究挑战为核心驱动力的,生物质谱技术的每一次突破,也加深了研究者对蛋白质结构和行为的理解。目前关于质谱技术的综述资源已非常丰富,读者可以借助各种途径获得相关知识。以下仅对蛋白质研究驱动的生物质谱技术做一概述。
1 生物质谱技术的前沿进展 1.1 离子化与离子淌度技术早期的离子化技术,通常采用电子轰击,这种所谓“硬”离子化方法,对于蛋白质或多肽这样连接键较弱的分子,往往过度碎裂而丢失了序列信息,因此质谱技术在其诞生后80年的时间里,对生物大分子的应用非常有限。1984年,John Fenn发明了电喷雾方法(electrospray ionization, ESI),1985年田中耕一发明了基质辅助激光解析离子化方法(matrix-assisted laser desorption ionization, MALDI),这两种被称为“软”离子化方法[2-3],对大分子尤其是蛋白质兼容,从此打开了生物质谱技术的大门,而这两位卓越的开拓者,也在2002年获得了诺贝尔化学奖。
针对生物大分子尤其是蛋白质,ESI和MALDI一直是主流的离子化方法。质谱前一定的液相色谱分离可提高灵敏度和分辨率,液相色谱-电喷雾离子化联用是有效的分离分析平台。为进一步提高灵敏度,还将纳升级流速的液相色谱与纳升喷雾相连。早期的液相进样往往在变性条件(如反相色谱中的乙腈洗脱)下,蛋白质的空间结构基本不会保留。为了解析蛋白质构象,发展了非变性质谱(native MS),即在接近生理条件下,蛋白质或蛋白质复合物进入电喷雾进行分析,其关键点是液相缓冲液既能保持蛋白质的构象,又不抑制电喷雾的效率。这一方法在蛋白质(如抗体药物)和蛋白质-药物复合物的结构解析中发挥重要作用 [4]。在复杂体系中,分子通过液相分离和离子化以后,仍然可能是混合物,此时已进入气相环境,在此条件下,添加电场驱动离子按一定规律迁移,称为离子淌度(ion mobility),从而进一步分离不同特性的离子,此方法相当于增加了一个维度的分离和信息,有助于复杂体系难以分辨的物质比如同分异构体或翻译后修饰的解析[5-6]。在ESI离子化相关技术大规模应用于蛋白质尤其是蛋白质组研究时,MALDI因其适用于固体样本,也很快找到了最合适的应用场景——质谱成像,将组织切片置于MALDI离子源,在激光激发下,部分分子离子化后,进行分子空间分布定量,目前成为空间蛋白质组学的一种关键技术[7]。ESI和MALDI都是在真空环境下工作,近年来,常压离子化技术(ambient ionization)的开发试图在自然大气压环境下完成离子化,比如解吸电喷雾离子化(desorption electrospray ionization, DESI)等[8],这类技术能快速有效地进行组织原位分析,在蛋白质质量成像等领域有应用潜力。
1.2 新型碰撞技术与Top-Down技术仅仅是检测蛋白质或多肽的分子量仍然不够,因为氨基酸的序列信息才是蛋白质或多肽的真正密码。研究者进一步针对蛋白质或多肽,在离子化至检测器的运动路程上,设计了碰撞室(collision cell),把蛋白质或多肽通过各种方法碎裂。完整分子量测定是一级质谱,测定的分子离子称为母离子(parent ion)。碰撞后的片段分子量测定是二级质谱,测定的片段离子称为子离子(daughter ion)。具备一级质谱和二级质谱功能的技术称为串联质谱技术(tandem mass spectrometry)。至此,蛋白质或多肽的完整分子量、碎裂片段的分子量都可以被检测到,从而实现了定性。当然,如果蛋白质序列上出现修饰(如磷酸化、糖基化),相应片段的质量会发生偏移,从而被质谱捕捉。碰撞碎裂方式有:惰性气体介导的碰撞诱导解离(collision induced dissociation, CID)和高能碰撞解离(high-energy dissociation, HCD)、电子碰撞诱导解离(electron capture dissociation, ECD和electron transfer dissociation, ETD)、光子碰撞诱导解离包括紫外光解离(ultraviolet photodissociation,UVPD)和红外多光子解离(infrared multiphotodissociation, IRMPD)等。这些碎裂方式各有偏好性,在肽链中产生不同位置断裂的片段[9]。另外,随着对整体蛋白质序列分析的需求增加,发展了自上而下(Top-Down)方法[10],即不进行蛋白质酶解,直接测定分子量和序列,这自然需要更强或更复杂的碎裂方法,一般会采用电子诱导解离或者光子诱导解离[11]。自上而下(Top-Down)方法与前述的非变性进样方式结合,在解析蛋白质-小分子相互作用等方面很有发展潜力[12]。
1.3 高分辨质量分析技术质量分析器的作用就是使得不同离子按一定规律得到分离,质谱的分辨率是一个重要的性能参数。常用的质量分析器包括四极杆(Quatrople)、离子阱(Ion trap)、飞行时间(TOF)、轨道阱(Orbitrap)、傅里叶回旋共振(FTICR)等类型[13]。对于蛋白质这种长链化合物,分子量越大,多样性越高,所需要的分辨率就越高。早期的高分辨质谱主要是磁质谱和傅里叶回旋共振(FTICR)质谱,但这类质谱的质量分析器造价和维护成本高,难以广泛使用。在21世纪初,蛋白质组研究推进之时,对通用小型化高分辨仪器的需求日益凸显。2005年,赛默飞(Thermo)公司的轨道阱分析器问世[14],它既具有高分辨能力,又小型化而便于使用,成为生物质谱仪史上划时代的技术。此后20年,轨道阱分析器相关技术不断升级,发展到100K~500K分辨率水平。飞行时间分析器也有完成高分辨的能力,理论上飞行管越长,分辨率就越高,但这无疑增加空间和控制上的困难。近年来,采用反射技术缩小尺寸,并在飞行管的温度稳定性上有一系列改进,使得TOF与轨道阱分析器并驾齐驱,可完成复杂体系的蛋白质非靶向定性和定量,形成了目前主流的高分辨生物质谱技术。三重四极杆虽然分辨率不高,但因其灵敏度和选择性的优势,在蛋白质和多肽靶向定量方面占有一席之地。
1.4 质谱谱图采集和解析技术由于质谱检测的质荷比范围有限,通常通过蛋白酶如胰蛋白酶将蛋白质切成小的多肽片段,每个肽段的定性完成后也就完成了蛋白质的定性,这一流程称为“bottom-up”——自下而上。早期质谱碎裂产生二级谱图方法主要是数据依赖采集(data-dependent acquisition, DDA)。也就是说,丰度高的离子先被捕获和碎裂得到二级谱图,然后再依次按丰度捕获其他离子。这种方式会带来一个问题,就是在蛋白质组复杂体系中,低丰度肽段难以捕获。近年来,针对这一难题,发展了非数据依赖采集(data-independent acquisition, DIA),即根据质荷比的窗口进行谱图采集,这样不仅兼顾了高丰度和低丰度肽段,还使得实验间的定性和定量重复性得以改善[15]。在复杂体系中,非数据依赖采集的窗口越小,速度越快,分辨率也就越高。因此,质谱仪的扫描速度也一再突破极限,目前已有超过200赫兹扫描速度的高分辨质谱仪出现,为蛋白质组复杂体系的解析提供强有力的支持[16]。
采集到肽段质谱谱图后,常用的方法是借助物种的基因组序列翻译出理论蛋白质数据库,通过质谱实验谱图和理论谱图的比对,确定多肽乃至蛋白质的序列。相关流程最关键是控制假阳性和提高匹配灵敏度。如果没有蛋白质序列的参考数据库,直接通过谱图进行序列分析,称为“从头测序”(de novo sequencing),这一过程准确度受谱图质量影响大,准确度不够高[17]。
1.5 面向蛋白质组复杂体系的质谱技术20世纪90年代后期,John Yates发展了鸟枪法(Shotgun)质谱技术,无须分离细胞蛋白质,而是将其混合物酶解成肽段,通过液相色谱分离后,再进入质谱进行定性和定量,这一策略很快得以推广并成为蛋白质组学的主流平台[18]。在蛋白质组复杂体系定性和定量需求的驱动下,生物质谱技术开始在分辨率、灵敏度、扫描速度和准确度方面快速更新迭代。随着研究的进展,研究者们意识到,蛋白质组的变化比想象的更多,对这些成分的定性就是一个挑战。比如已发现的几百种修饰如磷酸化、泛素化和糖基化等需要进行富集,才能在复杂样本中被定性和定量[19]。上千万个单氨基酸多态性位点(single amino-acid polymorphism, SAP)给每个蛋白质都增加了多样性和动态性,也要求质谱技术进一步提升其能力[20]。在复杂性很高的情况下,对每个蛋白质的氨基酸鉴定的覆盖率会降低,此时,可采用多酶合一的方法来增加对蛋白质和修饰的覆盖率[21]。不同物种、细胞、组织、体液的蛋白质组复杂性并不相同,比如血浆的蛋白质组种类很多,而且高丰度蛋白质如白蛋白会抑制低丰度蛋白质的检测,因此,血浆蛋白质组的研究深度目前还是一个挑战[22]。有趣的是,即便在高度混杂的背景情况下,高分辨质谱仍然能定性到特异肽段,我国科学家借助质谱技术确定了哈尔滨古人类化石中的蛋白质来自丹尼索瓦人[23],高灵敏度质谱技术发掘了穿越时空的蛋白质信号,为考古学做出了贡献。在定量水平,借助DIA采集模式可实现高覆盖非靶向定量,借助稳定同位素标记实现多重定量,借助多反应监测或平行反应监测完成靶向定量。
1.6 人工智能与生物质谱技术质谱仪扫描速度的加快,意味着海量图谱的产生,深度学习和人工智能最先应用的方向即是质谱谱图解析。比如DeepSearch采用Transformer提取肽段和谱图特征,引入对比学习框架,可以在零学习的情况下完成准确的肽段定性[24]。针对从头测序的准确度较低的问题,InstaNovo基于Transformer和扩散模型进行优化,显著提高了从头测序的准确度,在免疫肽、纳米抗体测序方面提升了性能[25],并拓展到对蛋白质修饰的分析。基于临床或疾病模型的样本分析会产生大量数据,人工智能辅助的识别在空间蛋白质组学方面也大有用武之地,PLATO通过迁移学习重构了空间蛋白质组分布[26]。“AI for Science”虽然刚刚起步,但因其在解决复杂体系问题和解析大数据方面的能力,必将和质谱技术结合,在生物医药领域发挥日益重要的作用[27]。
2 生物质谱技术应用热点和趋势 2.1 从蛋白质组到蛋白质网络蛋白质组学的研究深入到细胞层面后,蛋白质相互作用的研究越来越受到重视。细胞内的蛋白质不是单个起作用,而是通过与其他分子形成可调控的分子网络,分子网络的行为决定了最终的细胞行为。在此,蛋白质组学对质谱技术的要求更上一层,如何发现和定量蛋白质和其他分子间的相互作用成为新的研究前沿。由于细胞内的蛋白质与其他分子的相互作用往往是非共价的,非共价键在电喷雾质谱中难以保留。此时,化学生物学登场了,研究者们引入各种活性基团,发展了所谓生物正交反应(biorthogonal reaction),借助酶催化或光催化等方法实现邻近标记(proximity labeling, PL),在生理条件下快速原位标记蛋白质,再用质谱方法鉴定被标记的蛋白质,从而捕捉蛋白质相互作用或蛋白质亚细胞器成分[28-29]。也可采用各种化学交联方法,使蛋白质和其他分子交联起来,进一步结合质谱进行定性定量分析,即所谓交联质谱技术[30](crosslinking mass spectrometry, XL-MS),从而确定蛋白质-蛋白质、蛋白质-小分子、蛋白质-DNA、蛋白质-药物之间的相互作用[31-33]。目前,这方面的技术刚刚起步,还面临诸多问题,比如对复杂样本的交联效率、瞬时相互作用检测的准确性、对复杂数据的解读能力都有待提高。另一个充分利用质谱技术分析复杂体系的方向是诸如限制酶切质谱(limited proteolysis mass spectrometry, LiP-MS)等方法,将小分子与细胞或组织裂解液孵育,若小分子与蛋白质的某些区域结合,则酶切行为会发生变化,从而快速筛选出与小分子相互作用的蛋白质及区域[34],其筛选通量及对复杂体系的兼容度比其他方法更胜一筹。
2.2 从一级结构到高级结构自生物质谱技术出现以来,大多数工作集中在对蛋白质一级序列的分析,早期有零星的工作尝试用质谱技术进行结构生物学研究,比如用氢氘交换质谱技术(hydrogen deuterium exchange mass spectrometry, HDX-MS)研究蛋白质构象 [35],但相比其他结构生物学方法,质谱技术因对结构解析的精度有限,并非主流。然而,随着AlphaFold的横空出世,结构生物学的研究重点迅速从静态结构转到动态结构。人工智能的迅猛发展对数据规模提出要求。质谱技术因为通量高、速度快、对复杂样本容受度高,能较好适应上述需求,近两年相关技术得以发展,逐渐在蛋白质动态结构解析中占据更重要的地位。比如非变性质谱(native MS)分析在保留蛋白质空间结构的条件下,结合高能碰撞技术,进行序列和构象解析[36];羟基自由基蛋白质印迹技术(hydroxyl radical protein footprinting, HRPF)则通过对蛋白质进行快速氧化标记和检测[37],解析蛋白质的构象变化。蛋白质的群体行为是时间依赖的,即是高度动态的,比如蛋白质和小分子的结合往往在微秒到毫秒尺度已经发生和达到稳态,需要结合HDX、HRPF、电镜等各种不同时间尺度的方法来解析[38]。
2.3 从组织到单细胞空间分布随着质谱仪的扫描速度越来越快,通量越来越高,研究者们不再满足仅仅在完整组织水平定量蛋白质组,而是进一步追求揭示蛋白质组织空间定量分布,甚至单细胞水平的蛋白质组分析。基于蛋白质标记和电感耦合等离子体飞行时间(inductively coupled plasma TOF, ICP-TOF)的流式质谱技术可以实现单细胞靶向蛋白质的定量[39]。借助激光显微切割或单细胞分离制备平台,结合更灵敏的质谱检测技术,单细胞和空间蛋白质组非靶向分析已经不是梦想[40]。基于MALDI等方法的质谱成像也在分辨率上达到单细胞水平[41]。在临床组织上通过显微切割方法,结合高灵敏度高分辨质谱仪,已实现组织深度成像分析(deep visual proteomics, DVP),此方法已在遗传性肝病中绘制了单细胞分辨率的蛋白质毒性图谱[42]。目前的瓶颈在于质谱的通量还不足以达到全组织细胞覆盖。一旦解决通量和深度问题,单细胞空间蛋白质组学研究将大放异彩。
2.4 从实验室到临床精准医学的提出,把各种组学推到了临床研究技术的核心位置。以质谱为基础的蛋白质组学在生物标志物的发现、药物靶标的发现、干预治疗的评价等方面发挥重要作用。基于质谱定量的蛋白质组、磷酸化蛋白质组等在肿瘤分子分型中占据核心地位[43-44]。我们的工作发现,基于质谱定量的蛋白质-磷酸化蛋白质网络药物敏感性判别模型的准确度优于基因组突变判别。在CPTAC计划的支持下,美国目前已有30多种肿瘤组织的蛋白质组被诠释,加深了对肿瘤特征的了解,并推动了药物研发[45-46]。质谱技术直接与临床对接,甚至出现了床边质谱仪,在手术过程中通过质谱检测,帮助治疗决策[47]。
3 我国生物质谱技术的发展我国的生物质谱技术与国际上较为同步,尤其有意思的是,田中耕一第一次用英文发表基质辅助激光解析离子化的报告就是在中日会议上,可以说中国科学界在生物质谱技术最早的发展中已有所贡献。20世纪90年代后期,在中国科学院的支持下,中国科学院上海生物化学研究所夏其昌研究组引进了我国最早的液相色谱-质谱仪,在这台质谱仪上,曾嵘等完成了我国最早的蛋白质一级序列分析、蛋白质二硫键分析、蛋白质糖基化分析等开创性工作。2000年左右,中国科学院上海生命科学研究院构建了蛋白质组研究平台。2005年,高分辨轨道阱质谱仪问世,我国第一台仪器即在该平台启用。这些工作都为后来的蛋白质科学研究(上海)设施的建设打下了基础。2015年和2018年,蛋白质科学研究设施在上海和北京分别正式运行,北京设施和上海设施都配备了很强的生物质谱平台,十年来都取得了令人赞叹的成绩。其中上海设施的质谱分析系统已支撑科学家们取得了一系列重要的前沿科技成果(超过20篇Cell、Nature、Science论文)。例如,2025年,上海设施质谱系统与上海科技大学王皓鹏教授合作在Nature发表论文,基于质谱修饰分析技术,发现了免疫检查点LAG3的泛素化修饰及其功能[48];与中国科学院分子细胞科学卓越创新中心童明汉教授在Nature发表论文,基于交联质谱技术,解析了减数分裂DSB形成关键SPO11-TOP6BL复合物的结构特征[49];与上海科技大学水雯箐教授合作在Nature Chemical Biology发表论文,基于氢氘交换的结构质谱技术,揭示了GPCR的结构调控特征[50]。北京设施在肝癌蛋白质组研究等方面有所突破,贺福初教授团队领导启动了国际蛋白质组pi-HuB计划[51]。不过,我国在质谱仪器研发制造方面目前较落后,绝大多数蛋白质研究相关质谱仪依赖进口。
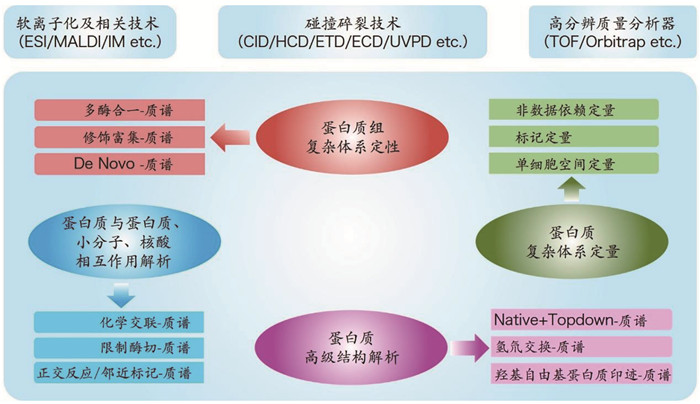
4 总结与展望图 2概括了蛋白质研究驱动的质谱技术内涵和前沿。作为生命功能的主要执行者,蛋白质的多样性、动态性和网络化恰恰是生命复杂性的基础,随着技术的进步,目前对蛋白质一级序列和静态空间结构的解析能力日趋成熟,而蛋白质动态结构解析这一难题则颇具挑战。此外,细胞内上万种蛋白质如何通过自组织完成随时空变化的群体行为,还是一个谜。相比其他研究方法需要纯化的蛋白质,质谱技术可以分析复杂样本,基于蛋白质标记或交联与质谱联用的技术也在朝着微秒尺度进步,未来的质谱技术应是研究蛋白质复杂动态行为的利器。另一方面,在临床应用中,蛋白质是核心的生物标志物和药物靶点,未来的质谱技术将更加强调高通量,可以对大人群进行多时间点的蛋白质定量监测,从而反映疾病发生发展和干预相关的个性化变化,在人工智能的辅助下,生物质谱技术将成为支持临床诊疗的关键技术。
|
图 2 蛋白质研究驱动的质谱技术内涵和前沿 |
一百多年前,当汤姆逊和阿斯顿使得阳离子偏转的时候,他们可能已经预料到这一技术的应用将深入到分子的各个层面。四十年前,当Fenn和田中耕一发现了适合生物大分子的离子化方式时,应是欣喜若狂,因为打开生物学的大门将意味着无穷无尽的可能。十年前,当蛋白质设施开始运行之时,生物质谱技术已成为蛋白质科学研究的重要工具。现在,我们将开启下一个和未来更多的十年,在复杂体系研究、临床研究和人工智能的发展浪潮中,我们有理由期待,生物质谱技术将应对更多挑战,也将不断突破边界。
| [1] |
Budzikiewicz H, Grigsby RD. Mass spectrometry and isotopes: a century of research and discussion. Mass Spectrom Rev, 2006, 25: 146-57. |
| [2] |
Fenn JB, Mann M, Meng CK, et al. Electrospray ionization for mass spectrometry of large biomolecules. Science, 1989, 246: 64-71. |
| [3] |
Tanaka K, Waki H, Ido Y, et al. Protein and polymer analyses up to m/z 100000 by laser ionization time-of-flight mass spectrometry. Mass Spectrom, 1988, 2: 151-3. |
| [4] |
Tamara S, den Boer MA, Heck AJR. High-resolution native mass spectrometry. Chem Rev, 2022, 122: 7269-326. |
| [5] |
Gabelica V, Marklund E. Fundamentals of ion mobility spectrometry. Curr Opin Chem Biol, 2018, 42: 51-9. |
| [6] |
May JC, McLean JA. Ion mobility-mass spectrometry: time-dispersive instrumentation. Anal Chem, 2015, 87: 1422-36. |
| [7] |
Caprioli RM, Farmer TB, Gile J. Molecular imaging of biological samples: localization of peptides and proteins using MALDI-TOF MS. Anal Chem, 1997, 69: 4751-60. |
| [8] |
Yang M, Unsihuay D, Hu H, et al. Nano-DESI mass spectrometry imaging of proteoforms in biological tissues with high spatial resolution. Anal Chem, 2023, 95: 5214-22. |
| [9] |
Guthals A, Bandeira N. Peptide identification by tandem mass spectrometry with alternate fragmentation modes. Mol Cell Proteomics, 2012, 11: 550-7. |
| [10] |
Lantz C, Wei B, Zhao B, et al. Native top-down mass spectrometry with collisionally activated dissociation yields higher-order structure information for protein complexes. J Am Chem Soc, 2022, 144: 21826-30. |
| [11] |
Xue JY, Liu ZY, Wang FJ. Applications of native mass spectrometry and ultraviolet photodissociation in protein structure and interaction analysis. Se Pu, 2024, 42: 681-92. |
| [12] |
Habeck T, Brown KA, Des Soye B, et al. Top-down mass spectrometry of native proteoforms and their complexes: a community study. Nat Methods, 2024, 21: 2388-96. |
| [13] |
Haag AM. Mass analyzers and mass spectrometers. Adv Exp Med Biol, 2016, 919: 157-69. |
| [14] |
Zubarev RA, Makarov A. Orbitrap mass spectrometry. Anal Chem, 2013, 85: 5288-96. |
| [15] |
Aebersold R, Bensimon A, Collins BC, et al. Applications and developments in targeted proteomics: from SRM to DIA/SWATH. Proteomics, 2016, 16: 2065-7. |
| [16] |
Guzman UH, Martinez-Val A, Ye Z, et al. Ultra-fast label-free quantification and comprehensive proteome coverage with narrow-window data-independent acquisition. Nat Biotechnol, 2024, 42: 1855-66. |
| [17] |
Vitorino R, Guedes S, Trindade F, et al. De novo sequencing of proteins by mass spectrometry. Expert Rev Proteomics, 2020, 17: 595-607. |
| [18] |
McCormack AL, Schieltz DM, Goode B, et al. Direct analysis and identification of proteins in mixtures by LC/MS/MS and database searching at the low-femtomole level. Anal Chem, 1997, 69: 767-76. |
| [19] |
Prus G, Hoegl A, Weinert BT, et al. Analysis and interpretation of protein post-translational modification site stoichiometry. Trends Biochem Sci, 2019, 44: 943-60. |
| [20] |
Gao X, Yin Y, Chen Y, et al. Uncovering dark mass in population proteomics: pan-analysis of single amino acid polymorphism relevant to cognition and aging. Cell Genom, 2025, 5: 100763. |
| [21] |
Gao X, Li Q, Liu Y, et al. Multi-in-one: multiple-proteases, one-hour-shot strategy for fast and high-coverage phosphoproteomic investigation. Anal Chem, 2020, 92: 8943-51. |
| [22] |
Soni RK. High-throughput plasma proteomic profiling. Methods Mol Biol, 2022, 2546: 411-20. |
| [23] |
Fu Q, Bai F, Rao H, et al. The proteome of the late Middle Pleistocene Harbin individual. Science, 2025, 18: eadu9677. |
| [24] |
Yu Y, Li M. Towards highly sensitive deep learning-based end-to-end database search for tandem mass spectrometry. Nat Machine Learning, 2025, 7: 85-95. |
| [25] |
Eloff K, Kalogeropoulos K, Mabona A, et al. InstaNovo enables diffusion-powered de novo peptide sequencing in large-scale proteomics experiments. Nat Mach Intell, 2025, 7: 565-79. |
| [26] |
Hu B, He R, Pang K, et al. High-resolution spatially resolved proteomics of complex tissues based on microfluidics and transfer learning. Cell, 2025, 188: 734-48. |
| [27] |
Mann M, Kumar C, Zeng WF, et al. Artificial intelligence for proteomics and biomarker discovery. Cell Syst, 2021, 12: 759-70. |
| [28] |
Huang Z, Liu Z, Xie X, et al. Bioorthogonal photocatalytic decaging-enabled mitochondrial proteomics. J Am Chem Soc, 2021, 143: 18714-20. |
| [29] |
Qin W, Cho KF, Cavanagh PE, et al. Deciphering molecular interactions by proximity labeling. Nat Methods, 2021, 18: 133-43. |
| [30] |
Botticelli L, Bakhtina AA, Kaiser NK, et al. Chemical cross-linking and mass spectrometry enabled systems-level structural biology. Curr Opin Struct Biol, 2024, 87: 102872. |
| [31] |
Yu C, Huang L. New advances in cross-linking mass spectrometry toward structural systems biology. Curr Opin Chem Biol, 2023, 76: 102357. |
| [32] |
Trendel J, Trendel S, Sha S, et al. The human proteome with direct physical access to DNA. Cell, 2025, S0092-8674(25)00507-0. |
| [33] |
Li K, Xie X, Gao R, et al. Spatiotemporal protein interactome profiling through condensation-enhanced photocrosslinking. Nat Chem, 2025, 17: 111-23. |
| [34] |
Malinovska L, Cappelletti V, Kohler D, et al. Proteome-wide structural changes measured with limited proteolysis-mass spectrometry: an advanced protocol for high-throughput applications. Nat Protoc, 2023, 18: 659-82. |
| [35] |
James EI, Murphree TA, Vorauer C, et al. Advances in hydrogen/deuterium exchange mass spectrometry and the pursuit of challenging biological systems. Chem Rev, 2022, 122: 7562-623. |
| [36] |
Britt HM, Ben-Younis A, Page N, et al. Conformation-specific approach to native top-down mass spectrometry. J Am Soc Mass Spectrom, 2024, 35: 3203-13. |
| [37] |
McKenzie-Coe A, Montes NS, Jones LM. Hydroxyl radical protein footprinting: a mass spectrometry-based structural method for studying the higher order structure of proteins. Chem Rev, 2022, 122: 7532-61. |
| [38] |
Du Y, Duc NM, Rasmussen SGF, et al. Assembly of a GPCR-G protein complex. Cell, 2019, 177: 1232-42. e11. |
| [39] |
Tajik M, Baharfar M, Donald WA. Single-cell mass spectrometry. Trends Biotechnol, 2022, 40: 1374-92. |
| [40] |
Bennett HM, Stephenson W, Rose CM, et al. Single-cell proteomics enabled by next-generation sequencing or mass spectrometry. Nat Methods, 2023, 20: 363-74. |
| [41] |
Taylor MJ, Lukowski JK, Anderton CR. Spatially resolved mass spectrometry at the single cell: recent innovations in proteomics and metabolomics. J Am Soc Mass Spectrom, 2021, 32: 872-94. |
| [42] |
Mund A, Coscia F, Kriston A, et al. Deep visual proteomics defines single-cell identity and heterogeneity. Nat Biotechnol, 2022, 40: 1231-40. |
| [43] |
Li C, Sun YD, Yu GY, et al. Integrated omics of metastatic colorectal cancer. Cancer Cell, 2020, 38: 734-47. |
| [44] |
Gao Q, Zhu H, Dong L, et al. Integrated proteogenomic characterization of HBV-related hepatocellular carcinoma. Cell, 2019, 179: 561-77. e22. |
| [45] |
Savage SR, Yi X, Lei JT, et al. Pan-cancer proteogenomics expands the landscape of therapeutic targets. Cell, 2024, 187: 4389-407. |
| [46] |
Petralia F, Ma W, Yaron TM, et al. Pan-cancer proteogenomics characterization of tumor immunity. Cell, 2024, 187: 1255-77. e27. |
| [47] |
Rappold BA. Clinical protein analysis by mass spectrometry: a new higher order. Clin Chem, 2021, 67: 461-2. |
| [48] |
Jiang Y, Dai A, Huang Y, et al. Ligand-induced ubiquitination unleashes LAG3 immune checkpoint function by hindering membrane sequestration of signaling motifs. Cell, 2025, 188: 2354-71. e18. |
| [49] |
Tang X, Hu Z, Ding J, et al. In vitro reconstitution of meiotic DNA double-strand-break formation. Nature, 2025, 639: 800-7. |
| [50] |
Zhang B, Ge W, Ma M, et al. Post-translational modifications orchestrate the intrinsic signaling bias of GPR52. Nat Chem Biol, 2025. DOI:10.1038/s41589-025-01864-w |
| [51] |
He F, Aebersold R, Baker MS, et al. pi-HuB: the proteomic navigator of the human body. Nature, 2024, 636: 322-31. |
 2025, Vol. 37
2025, Vol. 37 

 曾嵘,中国科学院上海高等研究院国家蛋白质科学研究(上海)设施副主任,上海科技大学/上海临床研究中心常任正教授。中国生物化学与分子生物学会分子系统生物学专业委员会副主任委员。曾嵘教授是我国生物质谱技术和蛋白质组学研究的开拓者之一。研究组目前的工作致力于发展基于系统生物学的精准医疗策略和基于组学大数据的疾病诊疗追踪与评价
曾嵘,中国科学院上海高等研究院国家蛋白质科学研究(上海)设施副主任,上海科技大学/上海临床研究中心常任正教授。中国生物化学与分子生物学会分子系统生物学专业委员会副主任委员。曾嵘教授是我国生物质谱技术和蛋白质组学研究的开拓者之一。研究组目前的工作致力于发展基于系统生物学的精准医疗策略和基于组学大数据的疾病诊疗追踪与评价