(2 上海科技大学,上海 201210)
(3 中国科学院上海高等研究院国家蛋白质科学研究(上海)设施,上海 201210)
(2 ShanghaiTech University, Shanghai 201210, China)
(3 National Facility for Protein Science in Shanghai, Shanghai Advanced Research Institute, Chinese Academy of Sciences, Shanghai 201210, China)
乙型肝炎是由乙型肝炎病毒(hepatitis B virus, HBV)感染引起的疾病,是全球公共卫生面临的严峻挑战。根据世界卫生组织(World Health Organization, WHO) 2024年的统计数据,全球约有2.54亿人处于慢性HBV感染状态,每年新增病例约120万例,相关死亡人数超过110万[1]。尽管已有广泛应用的预防性疫苗,乙型肝炎仍然是引发慢性肝炎、肝硬化以及肝细胞癌症的主要病因之一。
医学界对HBV的系统性认识始于19世纪中后叶,起初来源于临床实践中的偶然发现。当时,一些接受血清疫苗接种的群体出现了黄疸等典型肝炎症状[2-4],这一观察提示可能存在一种通过血液传播的未知病原体。然而,受限于当时病毒学技术的发展水平,该病原体的具体性质在相当长的一段时间内未能得到阐明。直到1964年,Blumberg等[5-7]在澳大利亚原住民的血清中首次发现一种可与多次输血治疗的血友病患者血清发生免疫反应的抗原,后被命名为“澳大利亚抗原”。1968年,Prince等[8, 9]进一步证实,该抗原与乙型肝炎患者血清中所检测到的“血清肝炎抗原”实为同一物质,并将其命名为乙型肝炎病毒表面抗原(hepatitis B surface antigen, HBsAg)。随后研究发现,这种抗原与肝炎密切相关,并包含直径约20 nm的球状及丝状颗粒[10],后被确认为亚病毒颗粒(subviral particles, SVP)[11]。这一发现不仅揭示了HBV的关键结构成分,也确立了HBsAg作为乙型肝炎诊断核心标志物的科学地位。
1.2 乙肝病毒表面抗原HBsAg由一个开放阅读框编码,通过不同的翻译起始位点生成小(S-HBsAg)、中(M-HBsAg)、大(L-HBsAg)三种类型的表面蛋白[12]。其中,S-HBsAg是病毒颗粒及SVP的主要组分,其羧基端的S结构域包含四个预测的跨膜螺旋结构,能够自发组装形成SVP,并携带诱导保护性免疫反应的关键抗原表位[13]。S结构域是三种异构体共有的结构区域,包含四个跨膜或膜结合螺旋,以及HBsAg的主要抗原决定簇,即“a”决定簇[14, 15],是当前疫苗设计的重要抗原表位。此外,S结构域中跨膜区域的动态构象变化可能影响病毒的组装与释放过程[16]。相比之下,M-HBsAg在N端增加了一个preS2结构域,而L-HBsAg则包含preS2与更长的preS1结构域。所有成熟的病毒颗粒中均含有少量(约10%) M-HBsAg,在丝状亚病毒颗粒和完整病毒颗粒中,L-HBsAg的含量约为25%;但在球形SVP中,L- HBsAg仅为痕量[12]。这种不同类型的HBsAg在不同颗粒间的分布差异提示其在病毒侵染和装配过程中可能具有特异性功能。值得关注的是,HBsAg在慢性HBV感染中可持续表达,且在某些情况下可整合入宿主基因组[17],这不仅加剧了病毒的免疫逃逸,还为乙型肝炎的彻底治愈带来了巨大挑战。
1.3 靶向乙肝病毒表面抗原的药物研发目前,慢性乙型肝炎的治疗主要依赖靶向HBV聚合酶的核苷酸类似物(如恩替卡韦、替诺福韦)和干扰素类药物。核苷酸类似物虽可长期抑制HBV复制、改善肝病进程,但难以清除HBsAg,干扰素类药物可实现部分患者HBsAg清除,但因副作用较大限制了广泛应用[18, 19]。
HBsAg的持续存在不仅反映病毒持续活动,更可导致免疫耐受,是功能性治愈的关键障碍。因此,近年来多项在研药物围绕降低HBsAg负荷展开,靶向机制主要包括:(1) HBsAg中和抗体,如VIR-3434[20]和lenvervimab[21],通过结合HBsAg阻断病毒入侵并介导免疫清除;(2)靶向HBV mRNA,小干扰RNA (small interfering RNA, siRNA)如VIR-2218[22]和JNJ-3989[23]、反义寡核苷酸(antisense oli-gonucleotides, ASO)如bepirovirsen[24],则是从翻译水平抑制HBsAg合成,联合干扰素治疗可显著提高清除率;(3) HBsAg分泌抑制剂,如REP 2139[25]通过干扰SVP的释放降低血液中HBsAg水平;(4)核心蛋白组装调节剂,如ABI-H0731[26]通过干扰病毒衣壳形成间接抑制HBsAg的生成;(5) HBV进入抑制剂,如Bulevirtide[27]通过阻断HBsAg与NTCP的结合而实现阻断病毒入侵,进而限制HBV感染扩散。这些创新疗法通过多途径协同降低HBsAg水平或限制其功能,不仅可能解除HBV介导的免疫抑制,更有望重建有效的适应性免疫应答,从而为突破HBV功能性治愈的瓶颈提供全新治疗范式。
1.4 乙肝病毒表面抗原的结构研究对HBsAg结构的观察与研究可追溯至20世纪60年代,1968年,Bayer等[28]用电子显微镜在患者血清中观察到了大量“澳大利亚抗原”组成的颗粒。1970年,Dane等[11]首次观察到血清中直径42 nm的完整病毒颗粒(Dane颗粒),证实了乙肝由典型病毒引起,同时也观察到了数量远超完整病毒颗粒的直径17~22 nm的球形与丝状亚病毒颗粒。1985年,Aggerbeck等[29]采用多种电子显微技术与X射线散射对HBV SVP进行了观察,发现其表面由直径约7.5 nm的亚基排列组成,平均粒径约19 nm。此后,大量结构生物学家和病毒学家一直致力于解析HBsAg结构及其在亚病毒颗粒与完整病毒颗粒上的分布。2005年,Gilbert等[30]利用冷冻电镜技术获得了分辨率为12 Å的重组HBsAg亚病毒颗粒结构,结果显示其具有正八面体对称性且疑似以HBsAg同源二聚体为构成单元。2006年,Yeager团队[31]利用冷冻电镜技术对从患者血清中分离的Dane颗粒进行了结构研究,发现其内部核衣壳具有T=3和T=4两种二十面体对称组装形式,但外部包膜上的HBsAg却不遵循二十面体对称性排列。2009年,Crowther团队[32]利用冷冻电镜技术尝试解析来源于患者血清的HBsAg丝状亚病毒颗粒低分辨率结构,观察到其直径约250 Å的管状结构表面呈现出刺突样特征,HBsAg二聚体在膜表面以紧密堆叠的模式排列。2012年,赵勤俭团队[33]利用冷冻电镜和原子力显微镜分析了HBsAg重组表达疫苗的颗粒形态,认为其为正八面体结构。2019年,朱平、张景强、罗树红团队[34]共同利用冷冻电镜单颗粒分析技术对HBV携带者血清中分离的天然亚病毒颗粒进行了结构解析,获得了分辨率约为30 Å的重构结果,其中HBsAg在球形亚病毒颗粒表面呈现出不规则的尖刺状特征,与Dane颗粒和丝状亚病毒颗粒类似,提示HBsAg在完整病毒颗粒和亚病毒颗粒中可能具有统一的折叠形态。2022年,Joseph Che-Yen Wang团队[35]利用一类较小的(直径约17 nm)具有正八面体对称性的亚病毒颗粒,获得了约6.3 Å分辨率的重构结果。然而,病毒粒子的高度异质性以及HBsAg可以预见的分子柔性,使得解析HBsAg高分辨率结构以及其在病毒粒子表面的分布机制极端困难,其依旧是结构生物学和病毒学长期未解的谜题。
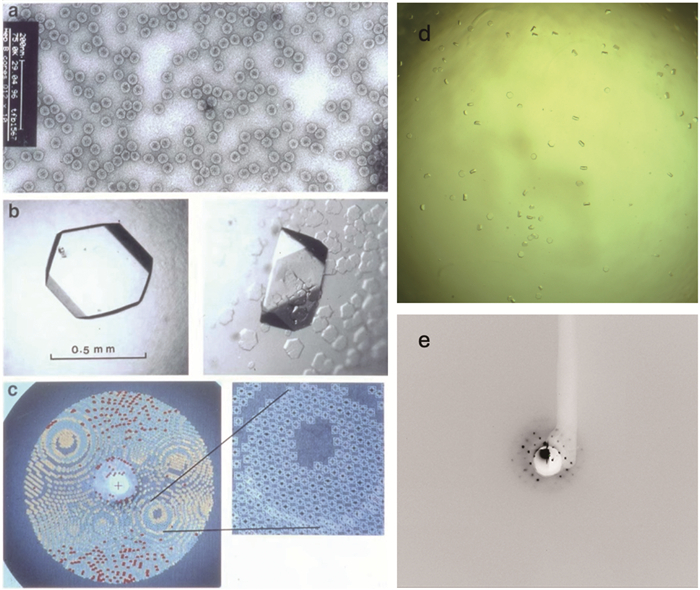
2 蛋白质设施支持乙肝病毒表面抗原结构研究的阶段性突破饶子和院士是我国著名的蛋白质科学和结构生物学家,早在英国牛津大学访学期间就成功获得了HBV核衣壳的蛋白质晶体(图 1a~c),并于二十年前与中国食品药品检定研究院的胡忠玉研究员合作尝试开展HBsAg的结构研究。在2007—2009年间,研究团队的傅晟博士等曾难得地获得了HBV SVP的晶体样品(图 1d、e),遗憾当时我国第三代同步辐射光源上海光源以及蛋白质设施的“五线六站”尚未投入使用,团队只得奔波前往英国钻石光源(Diamond Light Source)和日本高能加速器研究机构的光子工厂(Photon factory)开展衍射实验,但由于晶体内部分子依然存在的结构异质性,晶体衍射止步于纳米分辨率。2009年5月6日,蛋白质设施的蛋白质晶体结构分析系统正式对国内用户开放试运行,标志着我国蛋白质晶体学研究条件的极大提升。此后,对HBV SVP的晶体结构进行的持续研究,为理解SVP的几何特征提供了重要线索,也为后续利用冷冻电子显微分析开展研究做了样品准备。
|
a:HBV核衣壳的负染色电子显微照片;b:HBV核衣壳的晶体;c:HBV核衣壳的衍射图;d:HBV表面抗原亚病毒颗粒的晶体;e:HBV表面抗原亚病毒颗粒的衍射图 图 1 HBV核衣壳与表面抗原亚病毒颗粒的晶体 |
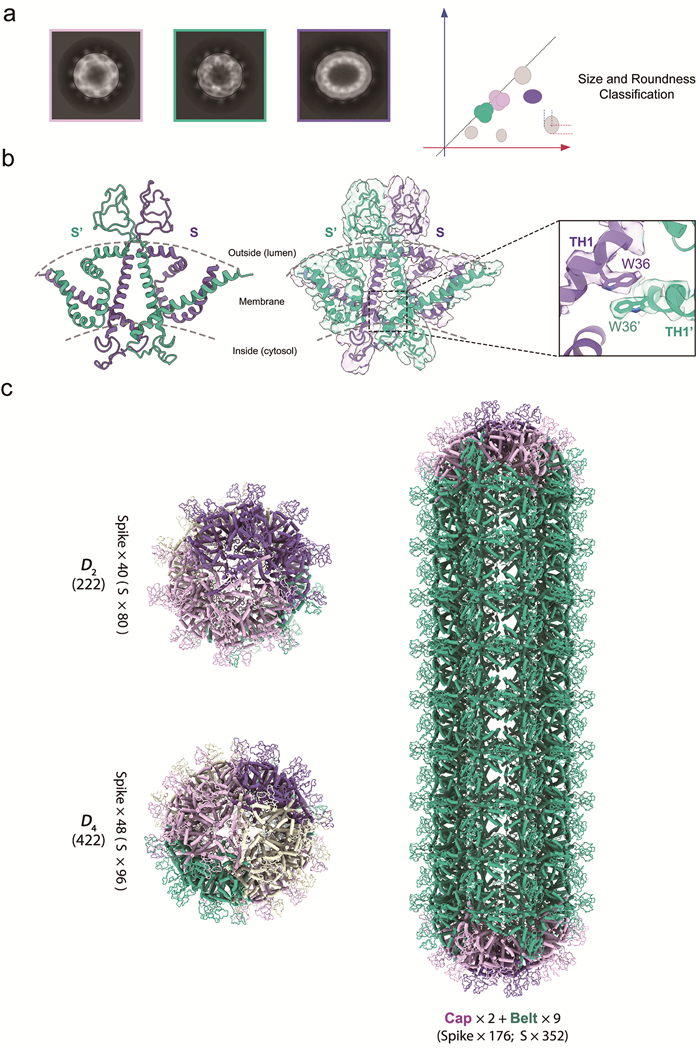
本文作者团队延续饶子和及胡忠玉老师的研究,尝试在上海科技大学和蛋白质设施利用冷冻电镜单颗粒分析技术来解析HBsAg结构。由于HBV SVP组装形式的高度异质性,在常规数据处理流程的二维分类(2D Classification)阶段,其二维平均图像呈现出尺寸与椭度迥异的颗粒形态(图 2a)。课题团队基于颗粒的投影特征开发了颗粒椭度筛选算法,通过从二维平均图像中提取颗粒边缘的采样点,拟合出最符合这些点分布的椭圆曲线以获得颗粒的长短轴估计(图 2a),从而分离出几何形态相对更接近正球的球形SVP (期待此类粒子具有更低的自由能状态,进而具有更为规整的结构形态),成功解析了由HBsAg同源二聚体组装而成的D2 (222)和D4 (422)两种准对称性22 nm SVP的亚纳米分辨率结构。基于D2准对称性SVP中HBsAg同源二聚体的组装形式,团队进一步使用改良的亚颗粒提取与平均方法,提取出SVP上每个HBsAg同源二聚体的颗粒图像信息,并根据其取向赋予初始对齐参数后进行局部搜索的对齐与重构,最终成功获得了分辨率为3.7 Å的HBsAg同源二聚体结构(图 2b)[36]。
|
a:HBV SVP二维平均图像椭圆拟合示例与正球形颗粒的分类筛选;b:HBsAg二聚体结构,其中对称单元的色氨酸残基(W36)在密度图中形成π-π堆叠相互作用;c:D2、D4及丝状SVP结构示意图。受D4 SVP结构启发,丝状SVP可能由围绕C4轴对称的两个半球冠与赤道部位的一个环带组成。通过在两极冠之间重复堆叠环带单元,进而形成直径22 nm的延伸丝状颗粒 图 2 HBsAg SVP同源二聚体结构与HBV SVP组装模型 |
该结构揭示了HBsAg S结构域的拓扑特征,包括2个氨基端跨膜螺旋、4个嵌膜螺旋、胞质环和内质网腔环区构成的复杂跨膜结构框架,特别是“a”抗原决定簇在空间结构中的暴露状态,为理解其免疫原性提供了直接证据。二聚体内部界面显示出由W36色氨酸介导的π–π堆叠、疏水嵌合及多个氢键网络,使其在动态膜环境中具有稳定装配能力(图 2b)。同时,通过对HBsAg多种构象的聚类分析,揭示其嵌膜螺旋区域存在显著的柔性构象异质性,提示HBsAg的二聚体具备进一步组装成不同寡聚体(如三聚体、四聚体)的构象适配性,为其装配多样亚病毒形态提供了结构基础。此外,基于其在SVP表面一种典型三聚体和三种不同四聚体局部组装模式的观察和分析,对球形SVP如何延展形成丝状SVP以及如何与内部核衣壳相适配组装形成完整病毒颗粒的分子机制进行了解读(图 2c)。
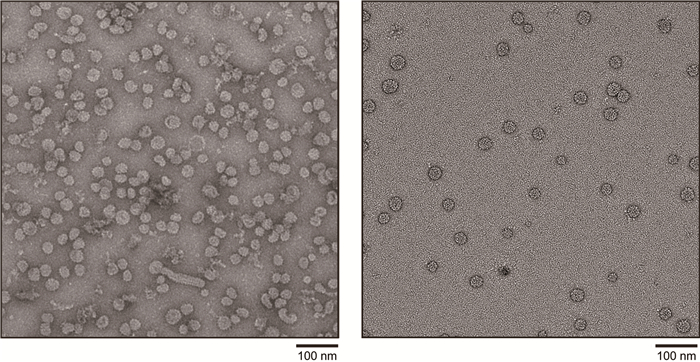
由于HBV颗粒组装形态的高度异质性,该研究前期需要不断评价粒子形态规律,并积累大量的冷冻电镜单颗粒数据,在此期间蛋白质设施的电镜分析系统为HBV结构研究提供了稳定的条件支持,该系统是国内唯一一个完全开放的标准、规范电子显微设施,能够提供高质量的电子显微分析。通过对HBV颗粒的电镜观察,研究团队系统评价了病毒颗粒的形态多样性,包括球形颗粒、丝状颗粒等,这些观察结果为后续的样品优化和结构解析提供了重要的线索(图 3)。与此同时,蛋白质设施的规模化蛋白质制备系统也为样品的表达和纯化及理化性质评价提供了丰富支持。通过这一系统,研究团队成功制备了高质量的HBsAg样品,并利用这些样品进行了病毒抗体识别与结合能力的评价,为理解HBsAg的免疫学特性提供了重要依据。
|
图 3 HBsAg亚病毒颗粒的负染色电子显微照片 |
尽管当前已获得HBsAg近原子分辨率的结构模型,但其构象异质性、寡聚体多样性及与核衣壳相互作用的结构基础尚未完全阐明,仍存在多个关键科学问题有待回答。
HBsAg的不同类型(S、M、L)在病毒包膜中的空间构象与功能分工尚不明确。未来可利用原位冷冻电子断层成像技术结合抗体或纳米抗体标记策略,对Dane颗粒进行原位电子显微成像,以观察preS1/preS2结构域的膜内外拓扑分布,以及其与核衣壳相互作用或与受体结合的结构特征。通过引入亚断层平均(subtomogram averaging)和针对性的三维分类算法,有望解析L-HBsAg在病毒生命周期中可能的双向拓扑转换的动态过程或多拓扑状态。同时,结合冷冻电子断层成像与光电联用显微技术(correlative light and electron microscopy, CLEM),可以在感染细胞环境中原位观察HBV包膜与核衣壳的组装过程,为深入理解HBV的感染机制与免疫逃逸策略提供动态结构视角。蛋白质设施已与中国科学院免疫与感染研究所合作建成国内第一个标准生物安全二级(BSL-2)防护的综合性电子显微设施,这为研究HBV的全病毒结构以及病毒在体感染状态的原位结构提供了重要的条件。
HBsAg的膜组分结合机制与装配路径仍有待厘清。利用蛋白质设施核磁分析系统的900 MHz高场Bio-NMR可对其跨膜螺旋与柔性环域在溶液中的构象动态进行监测,从而揭示其装配前后构象变化路径。质谱分析系统可对HBsAg的糖基化、二硫键修饰等翻译后修饰模式进行全面分析,明确这些修饰对抗原暴露、寡聚稳定性和免疫识别的影响。
目前乙肝功能性治愈的最大障碍之一在于HBsAg的持续表达与难以清除。随着HBsAg三维结构模型的建立,有望通过结构为基础的抗体筛选、小分子结合口袋识别、构象稳定诱导剂设计等方式,推动靶向HBsAg疗法的开发。结合结构信息的药物设计策略,亦可为RNA干扰疗法、蛋白降解靶向嵌合体(proteolysis-targeting chimera, PROTAC)或抗体药物及细胞免疫疗法的研发提供新的空间。结构生物学与药物化学、免疫学的交叉研究将成为未来乙肝治疗策略发展的重要方向。此外,HBsAg结构研究或许亦会为疫苗优化与开发提供新的契机,比如基于高分辨率结构信息,设计稳定构象的突变体或小分子结合剂,锁定关键装配界面或柔性区段,从而用于构象稳定的疫苗抗原制备。
蛋白质设施多系统联动构建了从分子分辨到细胞尺度、从构象变化到原位成像的完整技术链条,在支持HBV结构生物学研究方面已形成了高度集成的基础设施体系,这是蛋白质设施十年来支持我国蛋白质科学研究与技术方法创新蓬勃发展的一个缩影。未来,在蛋白质设施的持续支持下,HBV的相关研究有望取得更多突破,为全球公共卫生事业做出更大贡献。
| [1] |
World Health Organization. Global hepatitis report 2024: action for access in low-and middle-income countries[R]. 2024
|
| [2] |
Lurmen A. Eine lcterusepidemie. Berl Klin Wschr, 1885, 22: 20-3. |
| [3] |
MacCallum F. 1971 International symposium on viral hepatitis. Historical perspectives. Can Med Assoc J, 1972, 106(Spec Issue): s423-6. |
| [4] |
Seeff LB, Hoofnaglem JH, Norman JE, et al. A serologic follow-up of the 1942 epidemic of post-vaccination hepatitis in the United States army. N Engl J Med, 1987, 316: 965-70. |
| [5] |
Blumberg BS, Sutnick AI, London WT, et al. Hepatitis and leukemia: their relation to Australia antigen. Bull N Y Acad Med, 1968, 44: 1566. |
| [6] |
Blumberg BS. Polymorphisms of the serum proteins and the development of iso-preciptins in transfused patients. Bull N Y Acad Med, 1964, 40: 377. |
| [7] |
Blumberg BS, Gerstley BJ, Hungerford DA, et al. A serum antigen (Australia antigen) in Down′s syndrome, leukemia, and hepatitis. Ann Intern Med, 1967, 66: 924-31. |
| [8] |
Prince A. Relation of Australia and SH antigens. Lancet, 1968, 292: 462-3. |
| [9] |
Prince AM. An antigen detected in the blood during the incubation period of serum hepatitis. Proc Natl Acad Sci U S A, 1968, 60: 814-21. |
| [10] |
Millman I, Zavatone V, Gerstley BJ, et al. Australia antigen detected in the nuclei of liver cells of patients with viral hepatitis by the fluorescent antibody technique. Nature, 1969, 222: 181-4. |
| [11] |
Dane D, Cameron CH, Briggs M, et al. Virus-like particles in serum of patients with Australia-antigen-associated hepatitis. Lancet, 1970, 295: 695-8. |
| [12] |
Heermann KH, Goldmann U, Schwartz W, et al. Large surface proteins of hepatitis B virus containing the pre-s sequence. J Virol, 1984, 52: 396-402. |
| [13] |
Bertoletti A, Ferrari C. Adaptive immunity in HBV infection. J Hepatol, 2016, 64: S71-S83. |
| [14] |
Stirk H, Thornton JM, Howard CR, et al. A topological model for hepatitis B surface antigen. Intervirology, 1992, 33: 148-58. |
| [15] |
Brown SE, Howard CR, Zuckerman AJ, et al. Affinity of antibody responses in man to hepatitis B vaccine determined with synthetic peptides. Lancet, 1984, 324: 184-7. |
| [16] |
Le Seyec J, Chouteau P, Cannie I, et al. Role of the pre-S2 domain of the large envelope protein in hepatitis B virus assembly and infectivity. J Virol, 1998, 72: 5573-8. |
| [17] |
Levrero M, Zucman-Rossi J. Mechanisms of HBV-induced hepatocellular carcinoma. J Hepatol, 2016, 64: S84-101. |
| [18] |
Liu T, Wang H, Zhao Y, et al. Drug development for chronic hepatitis B functional cure: recent progress. World J Hepatol, 2025, 17: 105797. |
| [19] |
Tsai E. Review of current and potential treatments for chronic hepatitis B virus infection. Gastroenterol Hepatol (N Y), 2021, 17: 367-76. |
| [20] |
Agarwal A, Yuen MF, Wedemeyer H, et al. Dose-dependent durability of hepatitis B surface antigen reductions following administration of a single dose of VIR-3434, a novel neutralizing vaccinal monoclonal antibody. J Hepatol, 2022, 77(S1): S831-2. |
| [21] |
Kim JH, Kim HJ, Kim TH, et al. PS-077-Lenvervimab, a monoclonal antibody against HBsAg, can induce sustained HBsAg loss in a chronic hepatitis B mouse model. J Hepatol, 2019, 70: e50. |
| [22] |
Gane E, Lim YS, Tangkijvanich P, et al. Preliminary safety and antiviral activity of VIR-2218, an X-targeting HBV RNAi therapeutic, in chronic hepatitis B patients. J Hepatol, 2020, 73: S50-1. |
| [23] |
Yuen MF, Locamini S, Lim TH, et al. Short term RNA interference therapy in chronic hepatitis B using JNJ-3989 brings majority of patients to HBsAg < 100 IU/ml threshold. J Hepatol, 2019, 70: e51. |
| [24] |
Mak LY, Hui RWH, Fung J, et al. Bepirovirsen (GSK3228836) in chronic hepatitis B infection: an evaluation of phase Ⅱ progress. Expert Opin Invest Drugs, 2023, 32: 971-83. |
| [25] |
Bazinet M, Pantea V, Placinta G, et al. Safety and efficacy of 48 weeks REP 2139 or REP 2165, tenofovir disoproxil, and pegylated interferon alfa-2a in patients with chronic HBV infection naïve to nucleos (t) ide therapy. Gastroenterology, 2020, 158: 2180-94. |
| [26] |
Yuen MF, Agarwal K, Gane EJ, et al. Safety, pharmaco-kinetics, and antiviral effects of ABI-H0731, a hepatitis B virus core inhibitor: a randomised, placebo-controlled phase 1 trial. Lancet Gastroenterol Hepatol, 2020, 5: 152-66. |
| [27] |
Wedemeyer H, Aleman S, Brunetto MR, et al. A phase 3, randomized trial of bulevirtide in chronic hepatitis D. N Engl J Med, 2023, 389: 22-32. |
| [28] |
Bayer ME, Blumberg BS, Werner B. Particles associated with Australia antigen in the sera of patients with leukaemia, Down′s syndrome and hepatitis. Nature, 1968, 218: 1057-9. |
| [29] |
Aggerbeck LP, Peterson DL. Electron microscopic and solution X-ray scattering observations on the structure of hepatitis B surface antigen. Virology, 1985, 141: 155-61. |
| [30] |
Gilbert RJC, Beales L, Blond D, et al. Hepatitis B small surface antigen particles are octahedral. Proc Natl Acad Sci U S A, 2005, 102: 14783-8. DOI:10.1073/pnas.0505062102 |
| [31] |
Dryden KA, Wieland SF, Whitten-Bauer C, et al. Native hepatitis B virions and capsids visualized by electron cryomicroscopy. Mol Cell, 2006, 22: 843-50. |
| [32] |
Short JM, Chen S, Roseman AM, et al. Structure of hepatitis B surface antigen from subviral tubes determined by electron cryomicroscopy. J Mol Biol, 2009, 390: 135-41. |
| [33] |
Mulder AM, Carragher B, Towne V, et al. Toolbox for non-intrusive structural and functional analysis of recombinant VLP based vaccines: a case study with hepatitis B vaccine. PLoS One, 2012, 7: e33235. |
| [34] |
Cao J, Zhang J, Lu Y, et al. Cryo-EM structure of native spherical subviral particles isolated from HBV carriers. Virus Res, 2019, 259: 90-6. |
| [35] |
Liu H, Hong X, Menne S, et al. Cryo-EM structures of human hepatitis B and woodchuck hepatitis virus small spherical subviral particles. Sci Adv, 2022, 8: eabo4184. |
| [36] |
Wang Q, Wang T, Cao L, et al. Inherent symmetry and flexibility in hepatitis B virus subviral particles. Science, 2024, 385: 1217-24. |
 2025, Vol. 37
2025, Vol. 37 

 王权,上海科技大学生命科学与技术学院助理教授(Tenure-Track)、博士研究生导师,免疫化学研究所研究员。分别于2009年和2014年在南开大学获得计算科学学士学位和生物化学与分子生物学博士学位,毕业后进入中国科学院生物物理研究所工作,历任助理研究员、副研究员、研究员和青年课题组长。2014—2015年间曾赴英国牛津大学短暂访学,进行电子显微学技术方法的学习和研究。2020年2月加入上海科技大学至今,主要从事微生物病原体的跨尺度结构与功能研究
王权,上海科技大学生命科学与技术学院助理教授(Tenure-Track)、博士研究生导师,免疫化学研究所研究员。分别于2009年和2014年在南开大学获得计算科学学士学位和生物化学与分子生物学博士学位,毕业后进入中国科学院生物物理研究所工作,历任助理研究员、副研究员、研究员和青年课题组长。2014—2015年间曾赴英国牛津大学短暂访学,进行电子显微学技术方法的学习和研究。2020年2月加入上海科技大学至今,主要从事微生物病原体的跨尺度结构与功能研究