(2 上海科技大学,上海 201210)
(2 ShanghaiTech University, Shanghai 201210, China)
免疫受体是一组在免疫细胞表面表达的受体。作为免疫细胞表面精密分布的感受器,免疫受体构成了机体免疫监视系统的分子基础。这些结构多样的膜蛋白通过特异性识别外来抗原或内源性危险信号,精确调控免疫应答的启动、放大和终止,在维持免疫稳态中发挥着不可替代的作用。从功能上看,免疫受体呈现出令人惊叹的多样性:既有负责抗原特异性识别的T细胞抗原受体(T cell receptor, TCR)和B细胞抗原受体(B cell receptor, BCR),也包含调控信号强度的共刺激分子和抑制性检查点;既有介导细胞间通讯的细胞因子受体,也存在识别抗体Fc段或补体成分的特化受体。这种功能分化使得免疫系统能够对复杂多变的威胁做出恰当反应。对免疫受体调控机制的深入理解正在催生革命性的治疗策略。以2018年诺贝尔生理学或医学奖为代表的免疫检查点阻断疗法,通过解除程序性死亡受体1 (programmed death 1, PD-1)、细胞毒性T淋巴细胞相关抗原4 (cytotoxic T-lymphocyte-associated antigen 4, CTLA-4)等抑制性受体的刹车作用,显著提升了肿瘤免疫治疗的效果[1]。与此同时,合成生物学的发展使得工程化改造免疫受体成为可能,嵌合抗原受体T细胞(chimeric antigen receptor T-cell, CAR-T)疗法就是这一领域的杰出代表,通过赋予T细胞新的抗原识别能力开创了肿瘤治疗新纪元[2]。然而,当前免疫受体靶向治疗仍面临诸多挑战。在实体瘤治疗中,响应率不足的情况提示我们对受体调控网络的理解仍存在盲区;获得性耐药和治疗相关毒副作用也制约着临床获益。这些未满足的临床需求正驱动着基础研究的深入,从原子水平的受体构象变化,到细胞尺度的信号时空动态,再到组织微环境中的受体互作网络,多尺度的机制解析将为开发更安全有效的下一代免疫治疗奠定基础。在这个从实验室到病床的转化过程中,对免疫受体生物学的持续探索不仅将丰富免疫学理论体系,更可能为重大疾病的治疗带来新的突破。
免疫受体的核心功能在于将胞外配体刺激转化为胞内信号转导。在T细胞中,这一过程主要依赖于免疫受体胞内区酪氨酸(或丝氨酸/苏氨酸)的磷酸化修饰,这一保守机制确保了信号传递的精确性和可调控性。然而,在深入研究免疫受体信号转导的过程中,我们发现了一个长期被忽视却普遍存在的重要调控元件——碱性残基富集序列(basic-residue-rich sequence, BRS)基序。生物信息学分析显示约70%的人源单跨膜蛋白在其胞内近膜区都含有这一特征序列,包括关键的抗原受体(TCR、BCR)、共刺激分子(CD28)和免疫检查点(LAG3)等[3]。我们团队近年来系统研究了TCR、CD28和LAG3等多种免疫受体的活化机制,揭示了BRS基序在免疫受体全生命周期中的核心调控作用:从维持静息状态、动态调控配体识别、调控信号放大到信号抑制,这一看似简单的序列展现出显著的功能多样性。基于这些发现,本文将从三个维度深入探讨BRS基序的生物学意义:首先阐述BRS基序的发现历程及其基本特征;其次解析其通过静电相互作用动态调控免疫受体活化的分子机制;最后展望基于BRS基序编程的下一代细胞治疗策略,为精准免疫调控提供新理论和新思路。
1 BRS基序定义的提出免疫受体主要是单次跨膜蛋白,BRS基序在人源蛋白质组的单次跨膜蛋白中频繁出现[4]。全基因组分析揭示,约70% (1 269/1 818)的人源单次跨膜蛋白在其胞内近膜区携带净电荷≥+2的特征序列,这促使我们建立了BRS基序的明确定义:位于胞内近膜区、长度约10个氨基酸、净正电荷≥+2的功能模块(图 1A)[3]。序列特征分析显示,与胞外近膜区相比,这些区域呈现出显著的电荷不对称分布——富含碱性氨基酸精氨酸和赖氨酸而几乎不含酸性氨基酸天冬氨酸和谷氨酸。从结构动态学角度看,BRS基序展现出独特的构象可塑性:在溶液中表现为固有无序状态,而在膜结合时可被诱导折叠成两亲性螺旋,这种环境依赖的构象转变使其成为理想的信号转导调节元件。值得注意的是,虽然大多数BRS基序定位于胞内近膜区,但在某些特殊情况下可能分布在距离质膜更远端的位置(如TCR-CD3复合物中的CD3ζ链)[5]。本综述将重点讨论近膜区定位的BRS基序及其功能机制。
|
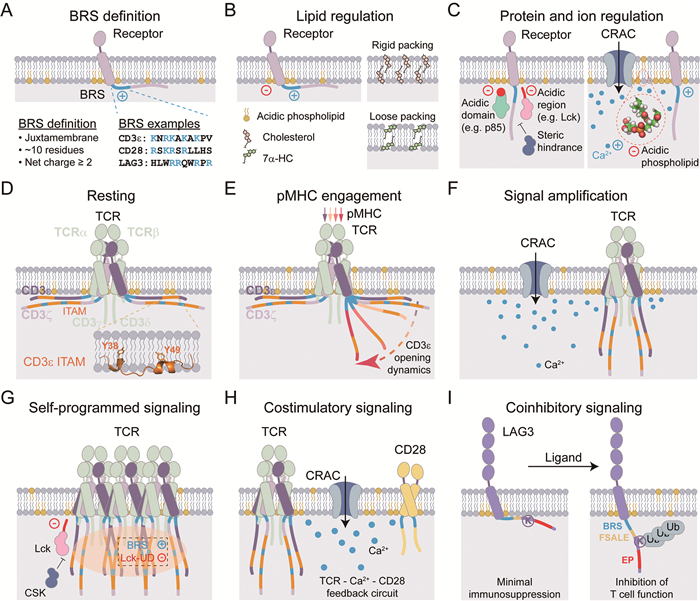
(A)BRS基序的定义。(B)基于脂质分子的BRS基序近膜静电调控网络。(C)基于蛋白质分子和金属离子等环境因素的BRS基序近膜静电调控网络。(D)静息状态下,TCR基于BRS基序的膜保护机制。(E)配体结合时,BRS基序调控的构象动态性是TCR转导不同刺激信号的结构基础。表示不同强度的pMHC的颜色与CD3ε构象的开放程度相对应。(F)基于BRS基序调控的TCR信号放大机制。(G)BRS基序调控的TCR信号放大和衰减的自编程机制。(H)共刺激受体CD28的TCR-Ca2+-CD28正反馈环路模型。(I)共抑制受体LAG3的“埋藏-释放”活化新机制。 图 1 碱性残基富集序列(BRS)介导的免疫受体信号转导机制 |
BRS基序作为免疫受体的关键调控元件,在胞内近膜区普遍存在并发挥重要功能。其特征性的高密度正电荷分布使其能够与周围带负电的分子形成动态的静电相互作用网络。这一调控网络具有显著的可塑性:在分子层面,可通过静电或非静电机制进行调节;在组成上,不仅包含膜脂质和信号蛋白等生物大分子,还整合了局部pH值和金属离子浓度等微环境因素,共同构成一个多维度的信号调控系统。
2.1 脂质分子细胞质膜的脂质分布具有显著的空间异质性,其内叶和外叶呈现截然不同的磷脂组成特征[6, 7]。质膜内叶富含带负电的磷脂,主要包括磷脂酰丝氨酸(PS,占比15%~30%),以及磷脂酰肌醇-4,5-二磷酸(PtdIns(4,5)P2,占比1%~2%);而外叶则以中性磷脂(如磷脂酰胆碱和鞘脂)为主。这种不对称分布为BRS基序的膜定位和功能调控提供了结构基础(图 1B)。研究发现,在TCR、BCR和细胞因子受体等免疫受体系统中,BRS基序通过多价静电作用与内叶酸性磷脂形成特异性互作网络:PtdIns(4,5)P2在受体周围局部富集,与BRS基序发生相分离,产生功能性纳米结构域[8];PS通过动态静电结合调控受体-膜相互作用,其浓度降低可诱导TCR-CD3复合物中CD3ε BRS基序从膜上解离[9]。这些发现揭示了酸性磷脂-BRS相互作用在免疫受体纳米簇形成和信号转导中的核心调控作用。
BRS基序的序列特征表现为碱性残基与疏水残基的协同分布。其碱性残基通过静电相互作用与膜脂质磷酸基团结合,而疏水残基则与脂质酰基链发生疏水相互作用,这种双重作用机制显著增强了BRS基序与质膜的结合稳定性。值得注意的是,无论是碱性残基还是疏水残基的突变,都会破坏这种精细的膜结合平衡[10]。有趣的是,虽然免疫受体胞内区在溶液中通常呈现固有无序状态,但在膜结合时会诱导形成两亲性螺旋结构:疏水残基插入脂双层疏水核心,而亲水残基(包括碱性残基)则稳定在膜界面区域[11, 12]。这种构象转变对BRS基序介导的信号转导具有关键的调控作用。
免疫受体与配体结合后发生寡聚化,形成富含胆固醇等刚性脂质分子的信号微簇。这些脂质微环境不仅能够稳定免疫受体-配体相互作用界面,同时会阻碍BRS基序及其邻近序列的膜插入(图 1B)[13]。值得注意的是,某些氧化型胆固醇(如7α-羟基胆固醇,7α-HC)表现出独特的调控作用:其C7位羟基的引入导致分子在脂双层中呈现倾斜取向,破坏脂质分子的紧密排列,从而在膜中产生结构间隙(图 1B)。这种局部膜结构的改变为BRS基序的膜插入创造了有利条件,最终实现对TCR信号通路的负向调控[14]。
2.2 蛋白质分子BRS基序的电荷相互作用网络不仅限于脂质分子,还包括多种蛋白质的酸性结构域。膜锚定酪氨酸激酶Lck通过其富含酸性残基的独特结构域(unique domain, UD)与CD3ε链BRS基序发生静电互作,这种互作不仅确保底物选择性,还显著提高了TCR磷酸化的效率[15]。值得注意的是,CD3ε的BRS邻近基序——脯氨酸富集序列(proline-rich sequences, PRS)和受体激酶(receptor kinase, RK)基序——可协同结合Lck的SH3结构域,形成多价相互作用网络[16]。类似地,磷脂酰肌醇3-激酶(PI3K)的p85亚基的酸性SH3结构域也能与CD3ε BRS基序建立静电互作(图 1C)[17]。除上述经典的电荷相互作用外,芳香族氨基酸的π电子云还可与BRS基序形成阳离子-π键,这一现象在含有多个酪氨酸的CAR分子中已得到实验证实[18, 19],因而拓展了BRS基序相互作用模式的多样性。
2.3 环境因素BRS基序的功能调控呈现出显著的环境依赖性,除脂质和蛋白质相互作用外,还受局部pH值和金属离子浓度等微环境因素的精细调节。以抑制性受体淋巴细胞活化基因3 (lymphocyte activation gene 3, LAG3)为例,其胞内区同时包含BRS基序和酸性谷氨酸-脯氨酸串联重复序列(EP基序)。在免疫突触形成过程中,EP基序通过释放质子降低局部微环境pH值,这一变化促使酪氨酸激酶Lck从共受体CD4/CD8上解离[20]。这种共受体-TCR信号通路的解偶联机制,最终导致T细胞活化受到有效抑制。
T细胞活化触发质膜钙释放激活的钙通道(Ca2+ release-activated Ca2+, CRAC)开放,导致钙离子内流[21]。这些内流的钙离子与CD3ε链及ζ链胞内区竞争结合膜内侧酸性磷脂,促使这些信号亚基从质膜解离(图 1C)[22]。随后,解离的CD3ε和ζ链被Lck磷酸化,进而增强TCR复合体的整体磷酸化水平。这一机制形成了TCR信号与钙离子流之间的正反馈循环,不仅有效放大初始信号,还能维持持续的TCR活化状态,最终显著提升T细胞对抗原刺激的响应灵敏度。
3 BRS基序的免疫受体信号调控机制BRS基序通过动态整合脂质、蛋白质及微环境信号,精密调控免疫受体功能的全生命周期(图 1D~I),具体包括静息态维持、信号启动、信号放大和信号抑制乃至终结。例如,在静息态,BRS-膜脂相互作用将关键信号基序(如磷酸化/泛素化位点)锚定在膜内侧,既维持受体结构稳定性,又有效阻遏非特异性激活。配体结合后,诱导BRS基序从膜上解离,引发双重效应:暴露的磷酸化位点招募Lck等激酶,开启信号转导;而暴露的赖氨酸残基可成为泛素化靶点,导致降解或通过泛素化依赖的信号转导调控受体活性。另一方面,BRS介导的相分离可形成信号枢纽,协同共刺激/共抑制分子构建调控网络,实现信号强度的时空精确控制。这种多层次的调控机制使BRS基序成为免疫受体功能可塑性的关键调控元件。
3.1 BRS基序对TCR全生命周期的调控机制TCR是T细胞活化和功能发挥的关键受体。TCR分子由抗原识别亚基TCRαβ和信号亚基CD3εγ、CD3εδ和CD3ζζ组成(图 1D)。抗原识别亚基TCRαβ的胞内区很短,因此TCRαβ需要与另外3个信号亚基结合来转导抗原刺激信号。3个信号亚基的胞内区总计有10个免疫受体酪氨酸活化模体(immunoreceptor tyrosine-based activation motif, ITAM)。在TCRαβ亚基识别抗原肽-主要组织相容性复合体(peptide-major histocompatibility complex, pMHC)后, 抗原刺激信号会被转导到CD3胞内区, 引发CD3亚基上的ITAM磷酸化,从而激活下游信号通路。除了ITAM基序以外,CD3ε亚基还含有BRS基序以及PRS和RK基序,CD3ζ亚基也含有BRS基序。下面将以CD3ε BRS基序为主线,阐述BRS基序在TCR各个生命过程中发挥的关键调控作用。
3.1.1 静息态下的膜保护机制T细胞表面表达多种免疫受体,包括抗原受体(TCR)及共刺激/共抑制分子(如CD28、PD-1等)。这些受体的信号转导均依赖于其胞内区信号基序中酪氨酸残基的可控磷酸化。常见的基于酪氨酸的胞内区信号模体包括ITAM、免疫受体酪氨酸抑制基序(immunoreceptor tyrosine-based inhibitory motif, ITIM),以及免疫受体酪氨酸开关基序(immunoreceptor tyrosine-based switch motif, ITSM)等[23, 24]。在静息状态下(配体未结合时),尽管激酶Lck在静息T细胞中持续表达,但ITAM等信号基序仅维持本底水平的磷酸化状态,表明应该存在安全保护机制,限制Lck对这些信号基序中酪氨酸的磷酸化,以有效防止信号的自发激活。
通过整合生物化学与生物物理技术,Xu等[11]揭示了TCR-CD3复合物中CD3ε亚基BRS基序的关键调控机制(图 1D)。研究发现,CD3ε胞内近膜区的BRS基序通过静电作用锚定于膜内层酸性磷脂,这一互作诱导ITAM形成独特的膜嵌入构象。CD3ε胞内区的核磁共振结构解析显示,蛋白质主链定位于脂双层界面,酪氨酸侧链插入膜疏水核心。这种“膜保护机制”有效抑制静息态T细胞的ITAM自发磷酸化。这项研究提出了静息状态下BRS基序对免疫受体的膜保护机制,为TCR的活化机制研究提供了新的思路。除了TCR信号转导以外,膜保护机制还适用于BCR[25]、共刺激受体CD28[4]、细胞因子受体IL-7R[26]、细胞程序性死亡-配体1 (programmed cell death ligand 1, PD-L1)[27]等免疫受体,提示这一机制对免疫受体的静息态维持具有普适性。
3.1.2 TCR复合物结构动态性调控抗原特异性免疫应答的新机制T细胞信号转导可分为三个阶段:抗原触发的初始活化阶段、信号放大阶段以及信号维持阶段[28]。如前所述,在静息态,CD3ε胞内区与膜结合,处于膜嵌入构象。在抗原刺激下,原本结合脂质的CD3ε胞内区必须从膜上解离并转变为“开放”构象,才能进行生化修饰或与下游分子结合。然而,CD3在抗原触发初始阶段如何实现构象开放至今仍未阐明。需要指出的是,简单的“闭合-开放”二元构象模型无法解释TCR的功能多样性。Guo等[10]由此提出假说:CD3胞内区可能存在多种中间构象状态,其功能基序可呈现不同的开放程度;具有不同TCR结合动力学的抗原可能通过稳定CD3胞内区的特定构象来触发差异化的下游信号转导。
为了验证上述假说,Guo等[10]首先开发了原子力显微镜(atomic force microscopy, AFM)单分子检测系统,用于研究CD3ε胞内区从闭合到开放的构象转变。AFM实验数据显示,除单峰力事件外,还观察到一定比例的双峰力事件,这表明CD3ε胞内区存在次级脂质结合位点。由于BRS基序是主要结合位点,次级结合位点应位于CD3ε胞内区的中段区域。通过核磁共振波谱技术——特别是溶剂顺磁弛豫增强(solvent paramagnetic resonance enhancement, sPRE)实验[29],研究人员在原子分辨率水平解析了CD3ε胞内区的构象动态特征。结果发现,CD3ε胞内区不同区段呈现异质性的脂质依赖动态特性,这为多种中间构象状态的存在提供了结构基础。此外,活细胞成像实验进一步验证了不同强度的抗原刺激诱导CD3ε展现不同程度的开放构象的生理相关性(图 1E)。本研究由此揭示膜脂依赖的TCR复合物构象动态特征很可能是TCR转导不同刺激信号的结构基础。
3.1.3 T细胞信号放大机制当TCR与pMHC结合后,能够触发全面的下游信号网络从而激活T细胞。其中,钙离子内流是TCR信号转导的早期标志性事件[21, 30]。研究报道,T细胞中主要的钙离子通道——CRAC与TCR在免疫突触中共定位。当钙通道开放时,钙离子快速内流,在开放通道周围形成高浓度钙微区。Shi等[22]通过核磁共振方法监测磷脂中磷的化学位移发现,生理浓度的钙离子可直接结合酸性磷脂的磷酸基团并扰动磷信号,但不能与双亲性磷脂结合(图 1F)。这种钙-磷酸基团的结合会中和磷脂负电荷,从而破坏CD3ε BRS基序与酸性磷脂间的静电相互作用。细胞实验证实,钙内流确实能显著增强活化T细胞中CD3ε的磷酸化水平。鉴于钙离子作为多功能信号分子可能通过其他途径影响CD3磷酸化,他们采用非信号转导的二价阳离子锶(Sr2+)进行对照实验。结果显示,Sr2+同样能通过CRAC通道内流,诱导CD3ε胞内区膜解离并促进其磷酸化,证明该过程仅依赖阳离子电荷而非钙特异性信号。需特别指出的是,CRAC通道仅在TCR初始触发后开放,因此钙内流对TCR磷酸化的增强作用主要发生在信号放大阶段。这种TCR-钙离子正反馈调控对T细胞功能至关重要——由于外源抗原生理浓度通常极低,初始TCR触发信号往往较弱,钙离子介导的TCR磷酸化正反馈机制可以有效地放大并维持TCR信号转导,提高T细胞对抗原的敏感性。
3.1.4 TCR信号放大与衰减的自编程调控机制在T细胞活化过程中,TCR分子在细胞接触界面的簇集及免疫突触(immunological synapse, IS)的形成是一个关键事件[31]。相较于TCR,CAR分子的簇集效率和免疫突触形成能力较弱,这一差异提示CD3ε、δ和γ亚基可能特异性地调控TCR的分子聚集机制。Chen等[18]利用二维膜系统(supported lipid bilayer, SLB)进行研究,发现在TCR-CD3复合物中,只有CD3ε的胞内区能够与激酶Lck发生相分离。这一过程依赖于CD3ε胞内区的BRS序列和Lck的UD结构域之间的静电相互作用,从而在膜上形成动态的液-液相分离结构。这种相分离不仅增强了TCR的磷酸化水平,还进一步促进Lck的活化,形成正向信号放大环路。然而,T细胞的过度活化需要被精确调控。Wu等[17]的前期研究发现,磷酸化的CD3ε能够招募抑制性激酶Csk。Chen等[18]将Csk引入相分离体系,发现Csk通过竞争性结合CD3ε,将Lck从相分离体系中排出,同时促使活化的Lck恢复到非活化状态,从而有效抑制T细胞的过度激活。这些结果综合表明,TCR信号调控呈现出一种自编程的动态平衡机制:一方面,CD3ε与Lck的相分离促进TCR簇集和信号放大,推动T细胞活化;另一方面,Csk的介入打破这一相分离体系,终止信号转导,防止过度活化。这种基于CD3ε/Lck的相分离与解离的调控闭环,确保了T细胞在抗原刺激下既能高效响应,又能适时回归静息状态,维持免疫反应的精准性与可控性(图 1G)。
3.2 共刺激受体CD28的活性调控机制CD28是T细胞中关键的共刺激受体,T细胞的完全活化依赖于TCR提供的抗原刺激信号和共刺激受体提供的共刺激信号。CD28的信号转导依赖于其胞内区的41个氨基酸残基,其中包含BRS基序以及提供酪氨酸磷酸化位点的PMNM和PYAP信号基序。CD28信号具有TCR依赖性,然而,这种信号依赖性的分子基础尚未完全阐明。
在静息态T细胞中,Yang等[4]发现,与TCR的情况类似,CD28中BRS基序的膜结合使其活性受限于膜结合状态。T细胞活化后,钙离子内流。钙成像实验显示,TCR信号诱导CD28周围形成局部钙离子富集区。核磁共振与荧光共振能量转移(FRET)检测表明,随着钙浓度升高,CD28与脂质的静电相互作用被破坏,其信号基序PMNM和PYAP中的酪氨酸侧链从膜内部解离。在原代T细胞功能实验中,TCR结合可显著增强CD28磷酸化,并促进下游信号蛋白(如p85、Lck和GRB2)的募集。这些结果共同证明钙离子通过电荷效应促进了CD28构象开放及信号转导。TCR诱导的钙内流解除了CD28膜结合的安全控制,导致CD28激活,这解释了CD28信号对TCR信号的依赖性。在3.3节已阐述的TCR与钙离子形成正反馈循环的基础上,该研究通过数学建模,进一步整合钙离子,提出了TCR-Ca2+-CD28的正反馈环路模型,指出这种正反馈环路模型可以迅速放大T细胞信号强度,从而极大地提高T细胞的抗原响应敏感性[4](图 1H)。
3.3 共抑制受体LAG3活化新机制LAG3作为一种重要的免疫检查点受体,在调控T细胞活化及抗肿瘤免疫应答中发挥关键作用。LAG3靶向药物于2023年获得美国FDA批准上市,是继PD-1和CTLA-4之后,第三个获批的免疫检查点药物[32]。尽管LAG3已成为癌症免疫治疗的重要靶点,但其配体结合后的激活机制尚未明确。
为探究LAG3受体的激活机制,Jiang等[33]利用蛋白质谱技术发现LAG3结合配体后,其K498位点发生快速多泛素化修饰。有趣的是,这种泛素化修饰不会介导LAG3的降解,反而对LAG3的功能具有关键作用。与其他免疫检查点受体不同,LAG3的胞内区缺乏典型的酪氨酸抑制基序。通过序列分选发现,LAG3近膜区含有进化上保守的BRS基序,紧随其后的是关键信号域FSALE以及泛素化位点[34]。利用生化实验和核磁共振波谱学等方法检测到,与TCR和CD28的情况类似,在静息态,LAG3的胞内关键信号域与膜脂互作,被埋藏在细胞膜中,从而隔离信号转导过程;当配体与LAG3受体结合后,泛素化修饰可促使LAG3胞内信号域从细胞膜中释放出来,从而有效激活LAG3的免疫检查点功能。这种由泛素化介导的“埋藏-释放”动态调控机制,揭示了一种全新的共抑制受体活化方式(图 1I)。基于上述LAG3激活机制的发现,Jiang等[33]对临床队列进行进一步分析,提出LAG3/CBL共表达可作为LAG3阻断治疗疗效的预测标志物,从而为靶向免疫检查点的精准治疗提供了新策略。
4 BRS基序在免疫细胞治疗中的应用过继性细胞治疗(adoptive cell therapy, ACT)作为肿瘤免疫治疗领域的重要突破,通过体外改造、激活和扩增患者自体免疫细胞(如T细胞、NK细胞等),再回输至患者体内,显著增强其识别和清除肿瘤细胞或病原体的能力。目前临床应用的ACT产品主要包括CAR-T细胞、工程化TCR-T细胞、肿瘤浸润淋巴细胞(TIL)以及自然杀伤(NK)细胞等,在恶性肿瘤、自身免疫性疾病和感染性疾病的治疗中展现出巨大潜力。研究表明,TCR信号强度是决定T细胞免疫应答质量的关键因素。这种信号转导具有双重调控特性:适度的TCR信号可促进T细胞活化和增殖,赋予其效应功能;而过强的信号则会导致T细胞终末分化,削弱其记忆性维持能力。因此,理想的T细胞治疗需要精确调控信号强度,在确保足够效应功能的同时,维持T细胞的干细胞样特性,从而实现持久且有效的免疫应答。基于对BRS基序调控免疫受体活化机制的深入理解,我们通过优化T细胞处理方案和改进分子构建等策略,对TCR-T和CAR-T疗法进行了系统性优化。这种精准的信号调控不仅显著增强了T细胞的体内持久性,更大幅提升了其抗肿瘤疗效,为开发新一代细胞治疗产品提供了重要理论基础和技术支撑。
4.1 TCR-T细胞治疗如前所述,BRS介导的信号转导可同时调控非抗原依赖性和抗原依赖性的TCR信号转导。在静息状态下,CD3ε的BRS结构域通过与质膜中的酸性磷脂相互作用,使CD3ε的BRS和ITAM基序嵌入膜内,从而有效抑制TCR的基底信号。Ren等[14]创新性地发现,通过添加7α-羟基胆固醇(7α-HC)可调控这一过程:该分子通过降低质膜脂质排列密度,在不影响细胞活力的前提下,显著增强了BRS与膜脂的相互作用(图 2A)。研究显示,在TCR-T细胞的体外扩增阶段进行7α-HC短暂处理,可有效降低T细胞的基底活化水平,显著提高记忆性T细胞亚群的比例(图 2B)。更重要的是,经7α-HC预处理的TCR-T细胞在持续抗原刺激条件下展现出显著增强的抗肿瘤功能,表现为:(1)体外扩增能力延长;(2)细胞耗竭程度减轻;(3)体内持久性提升。这一发现为通过精细调控TCR信号强度来优化T细胞治疗产品提供了新的技术路径,特别是为改善T细胞在慢性抗原刺激环境中的功能持续性提供了重要解决方案。
|
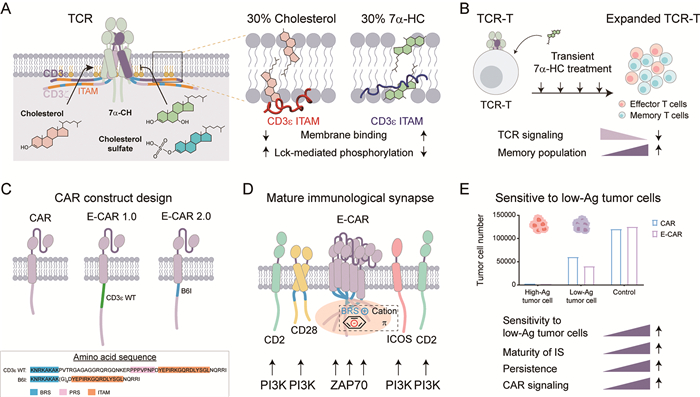
(A)胆固醇及其代谢物调控TCR信号转导的新机制。(B)羟基胆固醇短期处理提升TCR-T细胞的长效抗肿瘤功能。(C)利用BRS基序理性设计可相分离的E-CAR。(D) E-CAR促进T细胞免疫突触成熟。(E) E-CAR提高抗原敏感性和细胞长效性。 图 2 BRS基序在肿瘤免疫细胞治疗中的转化应用 |
与7α-HC的作用机制不同,胆固醇通过双重作用机制增强TCR信号转导:一方面破坏BRS结构域与膜脂的相互作用,另一方面促进TCR分子簇集。然而,肿瘤微环境(tumor microenvironment,TME)中的胆固醇代谢呈现显著失衡特征。Yan等[35]通过高分辨质谱分析发现,肿瘤浸润淋巴细胞(TILs)普遍存在胆固醇缺乏现象,而免疫抑制性髓系细胞和肿瘤细胞则表现出胆固醇过度累积。深入的甾醇组学研究揭示,TME中富含氧化型胆固醇代谢物(如27-羟基胆固醇和25-羟基胆固醇),这些代谢物通过抑制胆固醇摄取通路显著损害T细胞的胆固醇代谢稳态。机制研究表明,靶向敲除氧化型胆固醇的核受体LXR可部分恢复T细胞的胆固醇水平,并显著增强其抗肿瘤活性。另一方面,Yang等[36]研究发现,通过抑制胆固醇酯化酶ACAT1可阻止游离胆固醇向胆固醇酯的转化,从而维持TCR信号转导所需的膜游离胆固醇水平,促进T细胞增殖和功能维持。在多种临床前模型中,ACAT1抑制剂Avasimibe的系统性给药被证实能有效增强T细胞的抗肿瘤和抗病毒免疫功能,为改善肿瘤免疫治疗提供了新的代谢干预策略。
此外,在胆固醇衍生物中,天然代谢产物硫酸胆固醇(cholesterol sulfate, CS)是人类血浆中含量最丰富的硫酸固醇[37]。有研究表明,CS与胆固醇的相对比例决定了模型膜的相分离和膜曲率[38]。Wang等[39]发现CS可通过取代胆固醇而破坏TCR的聚集并抑制TCR信号转导(图 2A)。近来,Liang等[40]发现带负电的CS与带正电的CD3ε胞内区相互作用,增强了其与细胞膜的结合,并诱导形成稳定的二级结构,从而抑制TCR磷酸化。通过对CD3ε ITAM关键位点的突变设计,Liang等进一步构建了工程优化的TCR-T细胞;新构建的TCR-T细胞能够解除CS调控TCR的信号抑制,提升T细胞信号和抗肿瘤活性。该研究揭示了CS调控TCR信号的新机制,并为理性设计信号增强型TCR-T细胞提供了新策略。
4.2 CAR-T细胞治疗自20世纪80年代CAR-T细胞概念出现,研究者们致力于各种策略设计优化CAR分子,以提高CAR-T细胞的治疗效果。CAR-T细胞的疗效不仅取决于CAR对靶向细胞的亲和力,而且与CAR-T细胞的肿瘤杀伤力、增殖能力和长时间存活能力等特性息息相关。
鉴于CD3ε BRS基序通过对TCR信号放大与衰减闭环的调控功能,通过招募抑制型分子Csk抑制T细胞的过度活化,Wu等[17]创新性地将CD3ε结构域整合至临床批准的第二代CAR分子中,成功开发出更接近TCR功能特性的第一代E-CAR (即E-CAR 1.0)(图 2C)。研究发现E-CAR 1.0依然可以通过CD3ε招募Csk以及PI3K,并降低细胞因子分泌,促进细胞生长和存活,整体提高其持续性,使得抗肿瘤活性得到明显提升。此外,与常规二代CAR相比,E-CAR 1.0的胞内信号区展现出显著的液-液相分离特性,这一现象主要由CD3ε碱性氨基酸残基与信号区酪氨酸π电子间的阳离子-π相互作用所驱动。为进一步优化性能,Xu等[19]通过蛋白质工程改造构建了E-CAR 2.0 (又称EB6I CAR),在维持关键相分离位点的同时显著提高了膜表面表达水平(图 2C)。这种独特的相分离特性使E-CAR分子能够更有效地促进免疫突触的成熟:不仅增强中央超分子活化复合体(cSMAC)内的信号转导效率,还在突触外周形成更完善的CD2花冠结构,从而有效招募PI3K等信号分子传递共刺激信号,更好地整合了外源性E-CAR信号和内源性共刺激信号(图 2D)。这种设计不仅提升了免疫突触的质量,还显著增强了T细胞对弱抗原的敏感性并延长了细胞持久性,在动物模型中取得了显著的治疗效果,为CAR-T细胞疗法的优化提供了新思路(图 2E)。近年来,CAR分子设计的一个策略是引入TCR-CD3复合物中CD3ζ以外的其他CD3模块,以更好地模拟TCR的敏感性,并在受体下游激活类似的胞内信号转导网络[41, 42]。
5 总结与展望免疫受体的生理重要性和治疗潜力已广为人知,但其信号转导机制仍不甚明了。本文系统性地探讨了BRS基序在各种免疫受体中的作用,并阐述了BRS基序的信号转导机制和生物学功能。BRS基序因其集中的正电荷分布特征,能够与其环境形成动态电荷相互作用网络,从而调控免疫受体的磷酸化、泛素化、相分离等重要生命过程。
当前对BRS信号转导的认知仍存在重要知识缺口,亟待解决以下关键科学问题。首先是BRS基序的结构-功能相关性解析。虽然BRS蛋白以碱性残基富集为特征,但其成员间存在显著的序列异质性,表现在碱性残基的聚集/分散模式、是否含有酸性残基,以及其中所含的疏水残基的组成特征等方面。这些结构差异如何转化为功能特异性尚不明确,需通过系统的生物化学实验(如点突变结合功能表征)和计算生物学方法(如AI驱动的多尺度建模)建立结构-功能对应关系。其次是BRS信号在免疫治疗中的转化应用。鉴于BRS信号在免疫受体功能中的关键作用,可以开发调节这种信号的策略。与此相呼应,临床应用的异质性也对受体设计提出了差异化需求,即“情境适配型”设计理念。例如,在抗原稀缺场景,需要放大TCR信号,通过设计构建敏感型受体,优化免疫突触形成以识别低密度抗原;而在自发免疫病或需要长效效应的场景,则需要抑制TCR信号,以降低细胞因子分泌,并且促进细胞生长和存活,提高记忆性T细胞的比例,从而整体提高其持续性和治疗效果。BRS基序的广泛多样性为设计具有创新功能的新合成免疫受体提供了宝贵的资源。BRS基序作为免疫受体的关键调控元件,其分子机制和功能多样性仍有待深入探索。从基础机制解析到临床转化应用,亟需整合结构生物学、计算建模和免疫工程等多学科手段,以充分揭示电荷依赖性信号转导的调控规律,并开发基于BRS的精准免疫干预策略。
| [1] |
Ribas A, Wolchok JD. Cancer immunotherapy using checkpoint blockade. Science, 2018, 35: 1350-5. |
| [2] |
June CH, Sadelain M. Chimeric antigen receptor therapy. N Engl J Med, 2018, 379: 64-73. |
| [3] |
Shi X, He X, Xu C. Charge-based immunoreceptor signalling in health and disease. Nat Rev Immunol, 2025, 25: 298-311. |
| [4] |
Yang W, Pan W, Chen S, et al. Dynamic regulation of CD28 conformation and signaling by charged lipids and ions. Nat Struct Mol Biol, 2017, 24: 1081-92. |
| [5] |
Wu W, Yan C, Shi X, et al. Lipid in T-cell receptor transmembrane signaling. Prog Biophys Mol Biol, 2015, 118: 130-8. |
| [6] |
Wu W, Shi X, Xu C. Regulation of T cell signalling by membrane lipids. Nat Rev Immunol, 2016, 16: 690-701. |
| [7] |
Lorent JH, Levental KR, Ganesan L, et al. Plasma membranes are asymmetric in lipid unsaturation, packing and protein shape. Nat Chem Biol, 2020, 16: 644-52. |
| [8] |
van den Bogaart G, Meyenberg K, Risselada HJ, et al. Membrane protein sequestering by ionic protein-lipid interactions. Nature, 2011, 479: 552-5. |
| [9] |
Gagnon E, Schubert DA, Gordo S, et al. Local changes in lipid environment of TCR microclusters regulate membrane binding by the CD3epsilon cytoplasmic domain. J Exp Med, 2012, 209: 2423-39. |
| [10] |
Guo X, Yan C, Li H, et al. Lipid-dependent conformational dynamics underlie the functional versatility of T-cell receptor. Cell Res, 2017, 27: 505-25. |
| [11] |
Xu C, Gagnon E, Call ME, et al. Regulation of T cell receptor activation by dynamic membrane binding of the CD3epsilon cytoplasmic tyrosine-based motif. Cell, 2008, 135: 702-13. |
| [12] |
Duchardt E, Sigalov AB, Aivazian D, et al. Structure induction of the T-cell receptor zeta-chain upon lipid binding investigated by NMR spectroscopy. Chembiochem, 2007, 8: 820-7. |
| [13] |
Zech T, Ejsing CS, Gaus K, et al. Accumulation of raft lipids in T-cell plasma membrane domains engaged in TCR signalling. EMBO J, 2009, 28: 466-76. |
| [14] |
Ren Z, Wang K, Zhang Y, et al. Transient hydroxycholesterol treatment restrains TCR signaling to promote long-term immunity. Cell Chem Biol, 2024, 31: 920-31 e6. |
| [15] |
Li L, Guo X, Shi X, et al. Ionic CD3-Lck interaction regulates the initiation of T-cell receptor signaling. Proc Natl Acad Sci U S A, 2017, 114: E5891-9. |
| [16] |
Hartl FA, Beck-Garcia E, Woessner NM, et al. Noncanonical binding of Lck to CD3epsilon promotes TCR signaling and CAR function. Nat Immunol, 2020, 21: 902-13. |
| [17] |
Wu W, Zhou Q, Masubuchi T, et al. Multiple signaling roles of CD3epsilon and its application in CAR-T cell therapy. Cell, 2020, 182: 855-71.e23. |
| [18] |
Chen H, Xu X, Hu W, et al. Self-programmed dynamics of T cell receptor condensation. Proc Natl Acad Sci U S A, 2023, 120: e2217301120. DOI:10.1073/pnas.2217301120 |
| [19] |
Xu X, Chen H, Ren Z, et al. Phase separation of chimeric antigen receptor promotes immunological synapse maturation and persistent cytotoxicity. Immunity, 2024, 57: 2755-71.e8. |
| [20] |
Guy C, Mitrea DM, Chou PC, et al. LAG3 associates with TCR-CD3 complexes and suppresses signaling by driving co-receptor-Lck dissociation. Nat Immunol, 2022, 23: 757-67. |
| [21] |
Hogan PG, Lewis RS, Rao A. Molecular basis of calcium signaling in lymphocytes: STIM and ORAI. Annu Rev Immunol, 2010, 28: 491-533. |
| [22] |
Shi X, Bi Y, Yang W, et al. Ca2+ regulates T-cell receptor activation by modulating the charge property of lipids. Nature, 2013, 493: 111-5. |
| [23] |
Smith-Garvin JE, Koretzky GA, Jordan MS. T cell activation. Annu Rev Immunol, 2009, 27: 591-619. |
| [24] |
Fernandes RA, Su L, Nishiga Y, et al. Immune receptor inhibition through enforced phosphatase recruitment. Nature, 2020, 586: 779-84. |
| [25] |
Chen X, Pan W, Sui Y, et al. Acidic phospholipids govern the enhanced activation of IgG-B cell receptor. Nat Commun, 2015, 6: 8552. |
| [26] |
Moes B, Li H, Molina-Ortiz P, et al. INPP5K controls the dynamic structure and signaling of wild type and mutated, leukemia-associated IL7 receptors. Blood, 2023, 141: 1708-17. |
| [27] |
Wen M, Cao Y, Wu B, et al. PD-L1 degradation is regulated by electrostatic membrane association of its cytoplasmic domain. Nat Commun, 2021, 12: 5106. |
| [28] |
Courtney AH, Lo WL, Weiss A. TCR signaling: mechanisms of initiation and propagation. Trends Biochem Sci, 2018, 43: 108-23. |
| [29] |
Lenard AJ, Mulder FAA, Madl T. Solvent paramagnetic relaxation enhancement as a versatile method for studying structure and dynamics of biomolecular systems. Prog Nucl Magn Reson Spectrosc, 2022, 132-133: 113-39. |
| [30] |
Feske S. Calcium signalling in lymphocyte activation and disease. Nat Rev Immunol, 2007, 7: 690-702. |
| [31] |
Dustin ML, Choudhuri K. Signaling and polarized communication across the T cell immunological synapse. Annu Rev Cell Dev Biol, 2016, 32: 303-25. |
| [32] |
Aggarwal V, Workman CJ, Vignali DAA. LAG-3 as the third checkpoint inhibitor. Nat Immunol, 2023, 24: 1415-22. |
| [33] |
Jiang Y, Dai A, Huang Y, et al. Ligand-induced ubiquitination unleashes LAG3 immune checkpoint function by hindering membrane sequestration of signaling motifs. Cell, 2025, 188: 2354-71.e18. |
| [34] |
Andrews LP, Marciscano AE, Drake CG, et al. LAG3 (CD223) as a cancer immunotherapy target. Immunol Rev, 2017, 276: 80-96. |
| [35] |
Yan C, Zheng L, Jiang S, et al. Exhaustion-associated cholesterol deficiency dampens the cytotoxic arm of antitumor immunity. Cancer Cell, 2023, 41: 1276-93.e11. |
| [36] |
Yang W, Bai Y, Xiong Y, et al. Potentiating the antitumour response of CD8+ T cells by modulating cholesterol metabolism. Nature, 2016, 531: 651-5. |
| [37] |
Strott CA, Higashi Y. Cholesterol sulfate in human physiology: what′s it all about?. J Lipid Res, 2003, 44: 1268-78. |
| [38] |
Bacia K, Schwille P, Kurzchalia T. Sterol structure determines the separation of phases and the curvature of the liquid-ordered phase in model membranes. Proc Natl Acad Sci U S A, 2005, 102: 3272-7. DOI:10.1073/pnas.0408215102 |
| [39] |
Wang F, Beck-Garcia K, Zorzin C, et al. Inhibition of T cell receptor signaling by cholesterol sulfate, a naturally occurring derivative of membrane cholesterol. Nat Immunol, 2016, 17: 844-50. |
| [40] |
Liang W, Yi R, Wang W, et al. Enhancing the antitumor immunity of T cells by engineering the lipid-regulatory site of the TCR/CD3 complex. Cancer Immunol Res, 2023, 11: 93-108. |
| [41] |
Velasco Cardenas RM, Brandl SM, Melendez AV, et al. Harnessing CD3 diversity to optimize CAR T cells. Nat Immunol, 2023, 24: 2135-49. |
| [42] |
Minguet S, Maus MV, Schamel WW. From TCR fundamental research to innovative chimeric antigen receptor design. Nat Rev Immunol, 2025, 25: 212-24. |
 2025, Vol. 37
2025, Vol. 37 

 许琛琦,中国科学院分子细胞科学卓越创新中心(原生化细胞所)研究员。2004年毕业于中国科学院上海生命科学研究院生化细胞所,获得生物化学与分子生物学博士学位;2004‒2009年在哈佛大学医学院Dana-Farber肿瘤研究所从事博士后研究,后晋升为Instructor。2009年任职于中国科学院上海生命科学研究院生化细胞所,2020年至今任现职。实验室聚焦T细胞生物学研究,阐明抗原免疫应答调控新机制并发展肿瘤免疫治疗新策略。在Nature、Cell、Cancer Cell、Immunity等发表论文近100篇,成果入选2016年度中国科学十大进展及中国生命科学十大进展(2016、2020)。获得国家自然科学奖二等奖、上海市自然科学奖一等奖、科学探索奖、中国青年科技奖、尚思探索学者等科技奖项。国家杰出青年科学基金获得者,现任多细胞体系结构与功能重点实验室主任、中国生物化学与分子生物学会副理事长,Cell Research执行主编
许琛琦,中国科学院分子细胞科学卓越创新中心(原生化细胞所)研究员。2004年毕业于中国科学院上海生命科学研究院生化细胞所,获得生物化学与分子生物学博士学位;2004‒2009年在哈佛大学医学院Dana-Farber肿瘤研究所从事博士后研究,后晋升为Instructor。2009年任职于中国科学院上海生命科学研究院生化细胞所,2020年至今任现职。实验室聚焦T细胞生物学研究,阐明抗原免疫应答调控新机制并发展肿瘤免疫治疗新策略。在Nature、Cell、Cancer Cell、Immunity等发表论文近100篇,成果入选2016年度中国科学十大进展及中国生命科学十大进展(2016、2020)。获得国家自然科学奖二等奖、上海市自然科学奖一等奖、科学探索奖、中国青年科技奖、尚思探索学者等科技奖项。国家杰出青年科学基金获得者,现任多细胞体系结构与功能重点实验室主任、中国生物化学与分子生物学会副理事长,Cell Research执行主编