(2 美国罗格斯大学瓦克斯曼微生物研究所,新泽西州 皮斯卡塔维 08854)
(2 Waksman Institute of Microbiology, Rutgers University, Piscataway, NJ 08854, USA)
细胞内执行基因转录的RNA聚合酶(RNA polymerase, RNAP)根据亚基组成与功能特性,可分为单亚基RNAP和多亚基RNAP两大类。单亚基RNAP属于噬菌体类型RNAP,主要在真核细胞的细胞器(动植物细胞线粒体和植物前质体)中负责基因转录,这些单亚基RNAP由细胞核基因组编码,在细胞质中翻译后被运输到细胞器中发挥功能。多亚基RNAP包括细菌RNAP、古菌RNAP,真核生物的RNA Pol Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ[1-3] (其中RNA Pol Ⅳ/Ⅴ为植物所特有),以及植物质体基因组编码的RNAP (plastid-encoded polymerase, PEP)[3-5]。多亚基RNAP具有相对保守的催化核心,而古菌和真核生物的RNAP具有高度特化的多个外周亚基,赋予了它们不同的功能和调控机制,以适应其基因表达调控的复杂需求。下文将详细介绍多亚基RNAP结构的共性与特性,以及其转录与调控机制。
1 多亚基RNAP的三维结构 1.1 细菌RNAP三维结构细菌RNAP于20世纪60年代被发现,是研究最为深入的多亚基RNAP[6]。大肠杆菌RNAP核心酶(RNAP core enzyme)由五个亚基组成,包括两个α亚基(α2)、一个β亚基、一个β′亚基和一个ω亚基(图 1和表 1)。两个α亚基为装配亚基,帮助核心酶组装,并参与转录调控;β与β′为催化亚基,形成催化中心,负责RNA合成;ω亚基为辅助亚基,主要结合在β′亚基,稳定RNAP构象,并在转录过程中发挥调控作用[7]。细菌RNAP的整体形状像一个蟹爪,β和β′组成蟹爪的两个钳子,内部形成活性中心DNA通道,用来加载DNA。除了活性中心通道外,RNAP还含有两个额外通道,即NTP进入活性中心的二级通道(secondary channel),和新生RNA链退出的RNA退出通道(RNA exit channel)[7]。尽管RNAP核心酶具备合成RNA的催化活性,但其本身无法在基因特定位点起始转录。只有当RNAP核心酶与σ因子(σ factor)结合形成RNAP全酶(RNAP holoenzyme)后,才能特异性识别启动子DNA,并正确起始转录[8-10]。
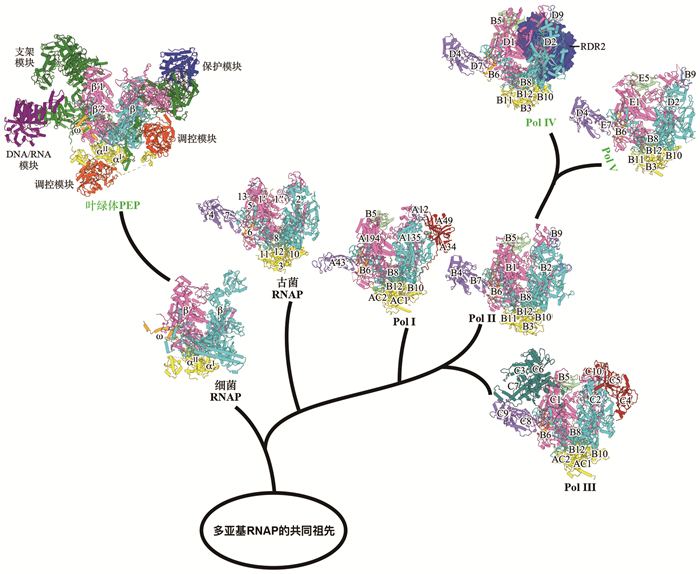
|
根据蛋白质结构数据库(PDB)中4MEY、8W9Z、3HKZ、7VBB、5IY7、7A6H、8XMC和8HYJ修改绘制。 图 1 多亚基RNAP的组成、结构以及进化关系 |
| 表 1 多亚基RNAP的组成 |
尽管RNAP的核心亚基高度保守,但在不同种属中,RNAP的亚基仍存在一些差异。在进化上较为古老的蓝细菌中,RNAP的最大亚基β′被拆分为两个亚基。蓝细菌RNAP结构表明,这种拆分并不改变其三维结构,拆分之后的两个亚基仍能正确组装成一个完整的β′亚基发挥功能[11]。此外,蓝细菌RNAP具有约630个氨基酸的插入序列(sequence insertion 3, SI3),约占全酶氨基酸总数的五分之一。该结构域自NTP通道延伸至DNA通道,在转录起始及延伸阶段发挥关键调控作用[11-12]。在革兰氏阳性菌枯草芽孢杆菌中,除核心的五个保守亚基(α2ββ′ω)外,RNAP还含有两个额外小亚基,分别为δ和ε。δ亚基在促进RNAP转录循环等方面发挥功能[13-14],而ε亚基可能在促进RNAP装配中发挥功能[15]。
1.2 叶绿体PEP的三维结构叶绿体是植物和藻类执行光合作用的关键细胞器,其起源可追溯至约15亿年前的蓝细菌内共生事件[16]。叶绿体基因组在内共生进化过程中大规模向核基因组转移或丢失,现今大多数陆地植物的叶绿体基因组仅保留110~130个基因,主要编码基因转录、蛋白质翻译、蛋白质降解、光合作用的蛋白质机器的核心组分[17]。叶绿体PEP在叶绿体从原质体向成熟叶绿体的分化过程以及分化成熟的叶绿体中承担主要的基因转录任务[4]。尽管叶绿体基因组在进化过程中大幅缩减,但其转录机器PEP却趋于复杂化。早前研究暗示PEP是由叶绿体基因组编码的核心酶亚基与十余种核基因组编码的PEP相关蛋白(PEP-associated proteins, PAPs)共同组成的分子量约为1 MDa的超大复合物。近期本实验室和其他实验室相继报道了PEP的高分辨率冷冻电镜结构[5, 18-20],结构表明PEP的核心由蓝细菌RNAP来源的亚基构成,形成“催化模块”,负责RNA的合成;而15种PAPs围绕核心模块组装成多个功能性模块,包括“支架模块”“保护模块”“DNA/RNA模块”“调控模块”,形成自然界已知最复杂的基因转录机器[5](图 1)。
“支架模块”由PAP1、PAP3、PAP5、PAP7、PAP8、PAP11和PAP14七个亚基组成,其直接与PEP“催化模块”发生相互作用,覆盖了PEP催化模块大部分表面,发挥组装和稳定“催化模块”的功能。此外,“支架模块”的亚基还为其他功能模块提供了结合到PEP核心“催化模块”的支架。“保护模块”由Fe-SOD异源二聚体(PAP4和PAP9,也称FSD3和FSD2)组成,该模块通过其超氧化物歧化酶(superoxide dismutase, SOD)活性,保护PEP免受叶绿体中活性氧(reactive oxygen species, ROS)的氧化损伤。“DNA/RNA模块”由PAP1和PAP2两个亚基组成,其中PAP1的DNA结合结构域能够结合并稳定下游双链DNA,PAP2结合于RNA退出通道附近,能够序列特异性地识别RNA,推测其参与RNA转录后加工。“调控模块”由PAP6、PAP13、两个PAP10和PAP15亚基组成,它们锁定PEP-α亚基C端结构域,可能参与PEP转录活性调控。上述功能模块均由细胞核基因组编码,在细胞质中翻译后转运至叶绿体,与PEP催化模块组装形成复合物,从而实现细胞核对叶绿体基因表达的精细调控。
1.3 古菌RNAP的三维结构古菌(Archaea)广泛分布于极端环境(如高温、高盐、高酸及厌氧环境)。近年来研究表明,部分古菌也存在于海洋、土壤及动物肠道等非极端环境。尽管古菌的基因排布方式和细菌类似,但是古菌RNAP的结构却与真核Pol Ⅱ高度同源[21-24]。
古菌RNAP由11~13个亚基组成,各亚基在RNAP的组装、催化及调控过程中发挥不同功能(图 1和表 1)。其中,Rpo3、Rpo11、Rpo10和Rpo12作为装配亚基(对应Pol Ⅱ的RPB3、RPB11、RPB10和RPB12),在RNAP组装中发挥核心作用;Rpo1′、Rpo1′′、Rpo2共同构成催化模块(对应于Pol Ⅱ的RPB1和RPB2),负责RNA合成;Rpo4和Rpo7形成Stalk结构域(对应Pol Ⅱ的RPB4和RPB7);Rpo5和Rpo6 (对应Pol Ⅱ的RPB5和RPB6)以及在某些物种中存在的Rpo8和Rpo13作为辅助亚基,参与RNAP的组装及活性调控[25]。由于古菌基因转录系统兼具真核RNAP结构特征和细菌基因调控特点,其独特性不仅使古菌成为研究基因转录调控的重要模型,也为深入理解真核生物的起源提供了重要的研究对象。
1.4 真核生物Pol Ⅰ~Ⅴ的三维结构细菌和古菌中只存在单一的RNAP,而大多数的真核生物细胞核中存在着三种RNAP:Pol Ⅰ、Pol Ⅱ和Pol Ⅲ[25-27]。Pol Ⅰ负责合成核糖体RNA (ribosome RNA, rRNA)前体,并进一步加工为28S、5.8S和18S rRNA;Pol Ⅱ负责合成信使RNA前体(messenger RNA, mRNA)以及非编码RNA (non-coding RNA, ncRNA),如miRNA、snRNA和小snoRNA等;Pol Ⅲ则负责合成短链非编码RNA,如转运RNA (transfer RNA, tRNA)、5S rRNA以及U6小核RNA等。
Pol Ⅰ、Ⅱ和Ⅲ均展现出保守的蟹爪型核心结构[27],并围绕这一核心结构搭载了数量不等的特异性亚基(图 1和表 1)。其中,人类细胞的Pol Ⅰ由13个亚基组成,Pol Ⅱ由12个亚基组成,Pol Ⅲ由17个亚基组成[2]。三种RNAP的核心结构均由10个与古菌RNAP同源的亚基构成[27],包括两个最大的催化亚基(Pol Ⅰ中为RPA194/RPA135,Pol Ⅱ中为RPB1/RPB2,Pol Ⅲ中为RPC1/RPC2)、一个参与校对的亚基(Pol Ⅰ中为RPA12,Pol Ⅱ中为RPB9,Pol Ⅲ中为RPC10)、五个共有亚基(RPAC1/2/3/4/5或RPB5/6/8/10/12),以及Pol Ⅰ/Ⅲ之间共用的RPAC1/ RPAC2 (Pol Ⅱ中为RPB3/RPB11)[28-30]。值得注意的是,三种RNAP的最大亚基的C末端结构域(C-terminal domain, CTD)具有较大区别。Pol Ⅱ最大亚基RPB1的CTD由保守的七肽重复序列Tyr1-Ser2-Pro3-Thr4-Ser5-Pro6-Ser7组成[31],重复数量从酵母的26个到人源的52个不等[32]。七肽序列上的氨基酸在转录过程中发生频繁的磷酸化与去磷酸化,调控RNAP的转录活性[33-34]。除核心亚基外,其他亚基对于相应的RNAP功能也非常重要。Pol Ⅱ的stalk模块包含RPB4和RPB7两个亚基(对应Pol Ⅰ的RPA43亚基和Pol Ⅲ的RPC9/RPC8亚基),其作为转录起始、延伸和终止因子的重要结合位点在整个转录过程中发挥关键作用[27, 30]。Pol Ⅰ和Ⅲ的部分亚基具有Pol Ⅱ通用转录因子类似的结构域,如Pol Ⅰ的RPA49/RPA34亚基(Pol Ⅲ中为RPC5/RPC4),与Pol Ⅱ的转录因子TFⅡF (α/β二聚体)结构相似[35-36],Pol Ⅲ的专属亚基RPC3/RPC6与Pol Ⅱ的转录因子TFⅡEα/β结构相似。Pol Ⅰ的RPA12亚基和Pol Ⅲ的RPC10亚基高度同源,由Pol Ⅱ的RPB9亚基与其转录延伸因子TFⅡS融合而成,在转录过程中具有校正功能,确保了延伸的高效和准确。以上结果暗示,Pol Ⅰ、Pol Ⅲ在演化过程中将Pol Ⅱ的通用转录因子整合为稳定亚基,实现其功能特化。
与其他真核生物不同的是,在高等植物中还存在着两类RNAP,分别为Pol Ⅳ和Pol Ⅴ[37],其主要功能是合成非编码RNA,通过RNA介导的DNA甲基化(RNA-directed DNA methylation, RdDM)途径建立和维持基因组DNA甲基化,沉默基因组的转座子活性。高等植物基因组含有大量的重复序列和转座子,如玉米和小麦基因组中的转座子含量高达80%[38],通过RdDM途径建立的DNA甲基化表观遗传修饰使转座子处于沉默状态,维持基因组的稳定[39]。RdDM通路主要分为两个步骤:(1) Pol Ⅳ和RNA依赖型聚合酶2 (RNA-dependent RNA polymerase 2, RDR2)协作在基因组特定区域(如转座子)合成双链RNA,随后该双链RNA被DCL3和HEN1加工修饰生成成熟的24 nt小干扰RNA (small interfering RNA, siRNA),并被AGONAUTE4/6 (AGO4/6)进一步切割保留单链;(2) Pol Ⅴ在相同区域转录RNA,而携带24 nt siRNA的AGO4/6蛋白通过两层相互作用定位到Pol Ⅴ的转录区域,第一层相互作用是AGO4/6蛋白和Pol Ⅴ之间的蛋白质相互作用,第二层相互作用是AGO4/6蛋白携带的24 nt siRNA与Pol Ⅴ的转录本发生碱基配对。两层相互作用的建立能够招募甲基转移酶DRM2对该基因组区域进行甲基化[3, 39]。
研究表明Pol Ⅳ和Pol Ⅴ由Pol Ⅱ演化而来,它们与Pol Ⅱ的亚基组成相似,与Pol Ⅱ共享部分亚基(RPB3/6/8/9/10/11/12)[40-41]。但是,Pol Ⅳ和Pol Ⅴ具有自己专属的亚基(Pol Ⅳ的专属亚基是NRPD1/5/7和RDR2;Pol Ⅴ的专属亚基是NRPE1/5/7)(图 1和表 1),这些亚基由Pol Ⅱ相应亚基的编码基因复制进化而来[42-45],赋予了Pol Ⅳ和Pol Ⅴ在细胞内的特殊功能。
2 细菌、古菌转录起始和终止机制 2.1 细菌RNAP转录起始机制转录起始是转录的第一步,也是最复杂的步骤。细菌RNAP核心酶需要与σ因子形成全酶才能精确起始基因转录[8-10]。细菌含有多种σ因子,不同类型的σ因子识别不同启动子序列,负责各自基因转录。根据结构和机制差异,细菌σ因子可分为两大家族:σ70家族和σ54家族。σ70家族成员较多,其包含细菌看家σ因子(如大肠杆菌σ70),负责大部分必需基因转录,还包含数量最多的ECF σ因子(extra-cytoplasmic σ factor),响应特定环境调控基因表达[46-47]。σ54家族成员较少,大多数细菌只编码1个σ54因子,其主要负责氮代谢、运动、生物膜形成等特定生理过程的基因转录。
RNAP与σ因子形成RNAP-σ全酶才具备识别基因启动子的能力。RNAP-σ70识别的启动子包含两个核心元件:-35区(5′-TTGACA-3′)和-10区(5′- TATAAT-3′),-35和-10区之间由16~19 bp的间隔区连接,其中最佳间隔为17 bp[8]。此外,部分启动子还包含额外调控元件,如UP元件(UP element: -40~-60区)、-10延长区(extended-10 element, EXT)、鉴别区(discriminator element, DISC)以及核心酶识别区(core recognition element, CRE),这些序列在不同程度上影响转录效率[8, 10]。RNAP-σ54识别的启动子核心元件则包括-24区(5′-TGGCAC-3′)和-12区(5′-TTGCT-3′)[48-49]。
RNAP-σ70的转录起始过程主要分为以下几个步骤:(1) RNAP-启动子DNA闭合复合物(RNAP-promoter DNA close complex, RPC):RNAP-σ70识别UP元件或-35区与启动子区形成闭合复合物[50](图 2A);(2) RNAP-启动子DNA中间复合物(RNAP-promoter DNA intermediate complexes, RPi):σ702结构域特异性识别启动子-10区,并逐步解链该区域,其中非模板链的-11A和-7T结合在相应的蛋白口袋中[50-51];(3) RNAP-启动子DNA开放复合物(RNAP- promoter open complex, RPo):RNAP将转录泡完全打开,将单链模板链DNA置于催化中心,形成稳定的开链复合物[50-53](图 2B);(4) RNAP-启动子DNA转录起始复合物(RNAP-promoter DNA initial transcription complexes, RPitc):RNAP起始RNA合成,产生productive product或abortive product;(5)启动子逃逸(promoter escape):当新生RNA延长至一定长度(10~15 nt)后,RNAP解离启动子DNA往前行进,进入转录延伸阶段[54-55]。RNAP-σECF全酶与RNAP-σ70全酶结构类似,且RNAP-σECF采用与RNAP-σ70类似的方式识别启动子DNA,但是σ70和σECF识别-35和-10区的氨基酸各不相同,因此二者能够识别不同序列的启动子DNA[56-58]。
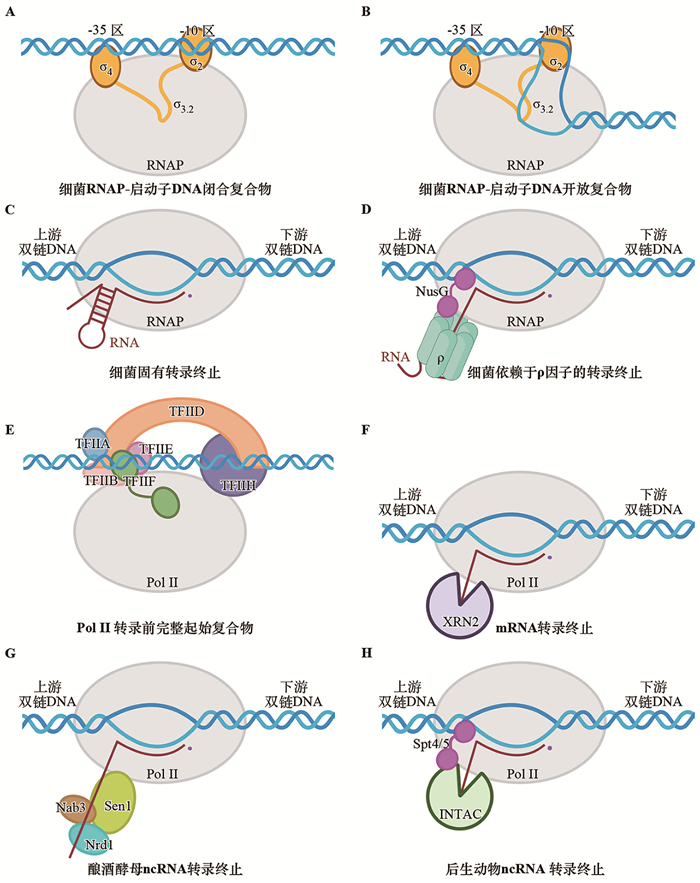
|
图片在https://BioRender.com绘制生成。 图 2 细菌和Pol Ⅱ转录起始与终止示意图 |
σ54与σ70在蛋白质序列上没有相似性。σ54由3个区段组成,区段Ⅰ由两个helix组成,参与DNA解链和转录泡形成;区段Ⅱ同样由两个helix组成,主要结合在RNA聚合酶内部;区段Ⅲ包含CBD (core binding domain)、ELH-HTH和RpoN三个结构域,其中ELH-HTH和RpoN分别负责识别-12区和-24区[48-49, 59]。不同于RNAP-σ70依赖型转录起始,RNAP-σ54结合启动子DNA形成闭合复合物后,无法自发形成开放复合物(RPo),而是需要远离启动子位点的ATP依赖型激活蛋白,也称为细菌增强子结合蛋白(bEBPs),解开双链DNA起始RNA合成[49, 60-61]。
2.2 细菌RNAP转录起始调控细菌主要通过σ因子和转录因子两个层面来调控转录起始。平均每种细菌编码大约10个σ因子,不同σ因子识别各异的启动子DNA核心序列调控基因表达。每种细菌还编码大量转录因子,例如大肠杆菌编码约300个转录因子(占总基因数量6%左右)。大多数转录因子含有DNA结合结构域(DNA-binding domain, DBD)和调控结构域(regulatory domain, RD),其通过特异性结合启动子,从而抑制或者促进RNA聚合酶与启动子DNA结合,实现转录抑制或者激活[62]。
细菌转录因子的激活方式复杂多样。根据作用机制,其可分为经典转录激活机制和非经典转录激活机制。经典转录激活机制按照转录因子结合在DNA的位置以及与RNAP-σ的相互作用方式可分为两类[63-65]。第一类(Class Ⅰ)转录因子结合在启动子DNA-35区上游,通过与RNAP-αCTD (RNAP-α C-terminal domain)相互作用招募RNAP,促进转录起始[66]。第二类(Class Ⅱ)转录因子结合位置与-35区部分重叠,其通过与RNAP-αCTD和σ70共同相互作用,促进转录起始[67]。
除了经典转录激活机制外,近年来多种非经典转录激活机制被报道。(1)改变DNA构象的转录激活。MerR家族转录因子在结合配体后,以二聚体形式结合在-35区与-10区之间,并通过弯曲和扭转DNA,将原本约19 bp的间隔优化为最佳的17 bp,从而促进RNAP的转录[15, 68-70]。(2)不依赖于DNA相互作用的转录激活。这类转录激活因子包括Crl、SutA、DksA、TraR和MgIA-SspA等[65, 71]。上述转录因子通过稳定RNAP转录各阶段结构,激活基因转录。调控σ54家族的转录因子也称为细菌增强子结合蛋白,其结合在核心启动子上游区域,在宿主整合因子(integration host factor, IHF)帮助下,利用ATP水解酶活性,重塑σ54、打开转录泡等[49, 60-61]。
2.3 细菌RNAP转录终止转录终止是RNAP停止RNA延伸,释放RNA,并从DNA上解离的过程[72]。细菌基因通过两种方式实现转录终止[72-74],一种是固有转录终止(intrinsic termination)或自发转录终止,也称不依赖ρ因子的转录终止;另一种是依赖于ρ因子的转录终止(ρ-dependent termination)(图 2C和D)。除此之外,还存在Mfd蛋白介导的转录终止以及近期发现的RNAP间碰撞介导的转录终止等其他形式[72-73, 75-78]。
固有转录终止是RNAP转录至固有终止子后自发终止转录的方式,是在所有细菌中均保守的转录终止方式[79]。固有转录终止子由一段富含G/C的发卡序列和紧跟其后的polyT序列组成。RNAP在polyT的第7或第8位发生终止[80-81]。固有转录终止分为4个步骤[82]。(1) polyU诱导转录暂停:RNAP转录至终止位点时,RNA链的polyU序列诱导RNA-DNA杂合双链在活性中心处于半移位非活性状态(即RNA链发生移位,而模板DNA链未发生移位),抑制NTP添加,从而暂停RNA延伸;(2) RNA发卡折叠:转录暂停为RNA发夹折叠提供时间窗口,RNA发卡折叠进入RNA退出通道,诱导RNA聚合酶构象变化,诱发转录泡闭合;(3) RNA-DNA杂合双链被破坏:RNA发卡进一步折叠,破坏RNAP催化中心RNA-DNA杂合双链,诱导RNA解离;(4) RNAP解离DNA:RNAP首先解离RNA,再从基因组DNA上脱离。部分细菌编码促转录终止因子帮助RNAP从基因组解离[82-84]。
依赖ρ因子的转录终止是RNAP在ρ因子的帮助下终止转录的方式。ρ因子通过结合富含嘧啶的rut (rho utilization, rut) RNA,并利用其ATP依赖的5′→3′ RNA转位酶活性,促使RNAP终止转录。ρ因子通过六聚体发挥功能[85]。ρ因子的转录终止过程大概分为4步[86]:(1) 处于开环状态的ρ因子识别并结合富含嘧啶的rut RNA;(2) ρ因子与rut RNA和ATP的结合诱导ρ闭环,激活ρ催化活性[87];(3) ρ因子水解ATP,沿5′→3′方向向RNAP移动;(4) ρ因子利用其转位酶活性,破坏RNAP活性中心RNA-DNA杂合双链,使RNA从RNAP中解离。在上述过程中,转录延伸因子NusG通过N端与RNAP结合、C端与ρ因子结合发挥桥梁作用,连接RNAP和ρ因子。在上述经典观点之外,一些研究提出ρ因子以转录延伸复合物为中心进行转录终止的新观点:在转录延伸过程中,ρ因子与转录延伸因子NusA和NusG协同作用,采取一种“搭便车”的方式先与RNAP结合,再捕获RNA,进而诱导RNAP发生一系列构象变化,进入失活状态,最终终止转录[13, 88-90]。
2.4 噬菌体蛋白抑制细菌RNAP转录终止噬菌体依赖宿主细菌来繁殖后代,其通常劫持宿主的RNAP转录自身基因,并抑制宿主基因转录[91]。此外,部分噬菌体编码抗终止蛋白,拮抗宿主RNAP转录终止,帮助噬菌体在合适的时间切换其基因组的早期基因到晚期基因的表达。
λ噬菌体N蛋白是第一个被报道的抗转录终止因子,开启噬菌体早期基因到中期基因的表达[92]。N蛋白识别RNA上的nut (N-utilization, nut)位点并结合转录延伸复合物,其活性需借助宿主Nus因子(NusA、NusB、NusE和NusG)。N蛋白与Nus因子形成复合物结合RNAP,阻止RNA发卡在RNA退出通道中形成,并稳定RNA-DNA杂合双链,抑制固有转录终止。NusE与NusG的C端结构域结合,阻断ρ因子与RNAP结合,从而抑制依赖ρ因子的转录终止[92]。λ和21噬菌体的Q蛋白开启从中期基因向后期基因的转录。Q蛋白和RNAP的复合物结构表明,Q蛋白在RNA出口通道形成环状结构,阻止RNA发卡生成,抑制终止[93-94]。Xp10噬菌体的P7蛋白是一种双功能调控因子,既可抑制宿主转录,又可促进噬菌体后期基因表达[95]。P7与RNAP的复合物结构表明,P7结合在RNAP的RNA退出通道,抑制RNA发卡在RNA退出通道形成,从而发挥抗终止作用[96]。
综上,这些噬菌体抗转录终止蛋白通过保守的机制拮抗转录终止,即结合在RNAP的RNA退出通道附近,阻止RNA发卡在RNA退出通道折叠,或者阻止终止蛋白ρ因子结合RNAP,从而抑制转录终止,开启噬菌体中后期基因的表达。
2.5 古菌RNAP转录起始机制细菌的RNA聚合酶启动转录时需要依赖σ因子,而古菌的RNAP则需要借助三种通用转录起始因子:TBP (TATA-binding protein, TBP)、TFB (transcription factor B, TFB)和TFE (transcription factor E, TFE),这三种因子分别与真核生物中的TBP、TFⅡB和TFⅡE具有同源性。古菌的启动子主要包括TATA box和BRE元件(B recognition element),其中TATA box通常位于转录起始位点上游-25 bp位置,是TBP的特异性结合位点,而BRE元件是TFB特异性结合位点。在转录起始过程中,TBP首先识别并结合TATA box,使局部DNA发生弯曲,随后TFB结合BRE元件,与TBP形成稳定的复合物,并招募RNAP,形成最小的DNA-TBP-TFB-RNAP转录起始前复合物。该复合物随后招募TFE,促进双链DNA的解链,形成转录起始开放复合物,起始RNA合成[22, 97-98]。由于缺乏完整的转录起始复合物三维结构,古菌的转录起始机制尚未阐明。
2.6 古菌RNAP转录终止机制古菌与细菌类似,主要存在两种转录终止途径:固有转录终止和FttA依赖型转录终止,此外还有Eta蛋白介导的转录终止。固有转录终止子的特征是非模板链中富含5~10个T的序列[98]。古菌转录终止因子FttA (factor terminates transcription in Archaea)也称作aCPSF1 (archaeal cleavage and polyadenylation specificity factor 1),负责古菌中大多数转录单元的转录终止。FttA特异性识别固有转录终止子的polyU序列[99],此外FttA具有核糖核酸内切酶活性和5′→3′核糖核酸外切酶活性[100-101]。转录延伸因子Spt5能够促进FttA的转录终止活性[100]。FttA转录终止复合物显示:FttA结合在RNA退出通道外侧,RNA从RNAP的RNA退出通道进入FttA的活性切割中心;Spt5的N端结构域结合RNAP,C端结构域结合FttA,在RNAP和FttA之间发挥桥梁的作用。FttA首先利用其核糖核酸内切酶活性切割RNA,然后利用5′→3′核糖核酸外切酶活性进行RNA 5′→3′切割和转位,最终破坏转录延伸复合物,引发转录终止[102]。
3 叶绿体PEP的转录起始与终止机制PEP的转录起始依赖于保守的启动子序列,典型启动子通常包含位于-35和-10区域的两个顺式元件,由PEP-σ全酶识别。植物细胞核通常编码多个σ因子,例如拟南芥编码6个σ因子(SIG1~6),负责在不同的发育阶段或者响应不同环境信号调控PEP转录活性。当前,PEP转录起始的具体分子机制仍需深入研究[4]。
PEP的转录终止机制也尚未阐明。部分叶绿体基因3′端存在可形成发卡结构的反向重复序列,但其主要功能可能在于稳定转录本、避免RNA降解,而非直接介导转录终止[103]。PEP是否通过类似细菌的固有转录终止机制终止转录有待进一步阐明。在拟南芥中,有研究表明RHON1参与rbcL与其下游基因accD之间的转录终止,然而具体机制未知[104]。
4 Pol Ⅱ转录起始和终止机制 4.1 Pol Ⅱ转录起始机制真核生物的转录起始尤为复杂,Pol Ⅱ需要在通用转录起始因子的帮助下才能识别基因启动子区域,并组装成转录起始前复合物(preinitiation complex, PIC)起始转录[105-108]。真核生物基因的核心启动子是一段以转录起始位点(transcription start site, TSS)为中心,上下游各长约50 bp的DNA序列。通用转录起始因子包括TFⅡD、TFⅡA、TFⅡB、TFⅡF、TFⅡE和TFⅡH[109]。通用转录起始因子与启动子DNA和Pol Ⅱ的结合存在时顺性,首先TFⅡD识别并结合至核心启动子,随后招募TFⅡA、TFⅡB、TFⅡF与Pol Ⅱ形成转录前核心起始复合物(core preinitiation complex, cPIC),接着招募TFⅡE形成转录前中间起始复合物(intermediate preinitiation complex, mPIC),最后招募TFⅡH形成转录前完整起始复合物(holo preinitiation complex, hPIC)(图 2E)。Pol Ⅱ转录起始活性能够被共激活因子Mediator进一步激活。Mediator促进PIC复合物组装的同时能够激活TFⅡH的CDK7激酶活性[110],对Pol Ⅱ CTD的Ser5进行磷酸化修饰,促进转录起始向转录延伸阶段转换。当组装成hPIC后,TFⅡH利用DNA移位酶的活性将DNA泵入Pol Ⅱ催化中心,并同时促进其解链形成转录泡。Pol Ⅱ起始RNA合成之后,随着RNA延长,不断增大转录泡的单链DNA以“蜷缩”(Scrunch)机制在催化中心积累挤压,TFⅡD的DNA移位酶活性进一步将下游DNA输泵入催化中心。当RNA长度到达10 nt之后,上述“蜷缩”过程积累的能量帮助Pol Ⅱ挣脱转录起始因子,进入转录延伸阶段[107]。
4.2 Pol Ⅱ转录终止机制Pol Ⅱ针对不同类型的RNA采用不同的转录终止机制[111]:Pol Ⅱ利用切割和多聚腺苷酸因子(cleavage and polyadenylation factor, CPF)和切割因子(cleavage factor, CF)途径(CPF-CF途径)终止mRNA转录;在单细胞真核生物酿酒酵母中,Pol Ⅱ利用Nrd1-Nab3-Sen1途径(NNS途径)终止ncRNA转录[2],在后生动物细胞中,Pol Ⅱ利用Integrator复合物终止ncRNA转录(图 2F~H)。
CPF-CF复合物识别富含腺嘌呤的多聚腺嘌呤位点(polyA site),并在下游区域切割、释放新生成的mRNA前体,随后mRNA前体添加polyA尾巴后被输送至细胞质中。Pol Ⅱ向前行进一小段距离后停止转录,Pol Ⅱ从基因组上解离,标志转录终止。目前关于Pol Ⅱ终止mRNA转录的机制存在着三种模型:鱼雷模型(torpedo model)、异构模型(allosteric model)和整合模型(sitting-duck torpedo model)[2]。鱼雷模型认为CPF-CF复合物切割mRNA后,残留RNA的5′端是5′→3′核酸外切酶(酿酒酵母Rat1、人XRN2、拟南芥XRN3)的识别和结合位点。当核酸外切酶结合RNA后,在切割RNA的同时追赶正在转录的Pol Ⅱ延伸复合物。当核酸外切酶追上Pol Ⅱ后,诱导Pol Ⅱ解离DNA和RNA[112]。异构模型认为,当Pol Ⅱ进入转录终止阶段后,转录延伸因子解离诱导Pol Ⅱ构象改变,促使Pol Ⅱ自发停止RNA合成,并解离DNA和RNA[113]。此外,近年来的整合模型认为Pol Ⅱ转录终止兼具异构模型和鱼雷模型的特征,在该模型中,CPF-CF切割mRNA后Pol Ⅱ构象发生变化,导致转录延伸速率下降,使得核酸外切酶能够追上行进中的Pol Ⅱ复合物,而Pol Ⅱ解离DNA和RNA的过程仍然依赖核酸外切酶[114]。
核酸外切酶介导的转录终止复合物三维结构显示,核酸外切酶稳定结合在Pol Ⅱ RNA退出通道外侧,其结合位置和转录延伸因子重叠,揭示核酸外切酶在转录终止阶段替换延伸因子,削弱Pol Ⅱ和RNA/DNA杂合双链的亲和力,减缓Pol Ⅱ转录速率。核酸外切酶直接将Pol Ⅱ转录的RNA 5′端引导至其催化中心,利用自身的RNA外切酶活性缩短RNA,最终诱导RNA从Pol Ⅱ活性中心解离。上述结构生物学证据支持Pol Ⅱ mRNA终止的整合模型。
酵母细胞ncRNA转录终止的NNS复合物由RNA结合蛋白Nrd1和Nab3以及核酸解旋酶Sen1组成。Nrd1和Nab3分别识别RNA上的特异转录终止序列GUAA/G和UCUUG以及Pol Ⅱ CTD丝氨酸磷酸化(Ser5P)信号,随后通过蛋白质间的相互作用招募Sen1蛋白至转录延伸复合物[115-116]。Sen1结合在Pol Ⅱ RNA退出通道附近,与RPB3亚基存在直接作用。Sen1终止机制与细菌ρ因子类似,利用自身5′→3′解旋酶功能释放聚合酶活性中心的RNA[116]。
在后生动物细胞中,转录起始后Pol Ⅱ通常会在TSS下游20~200 bp发生停顿,称为启动子近端暂停(promoter-proximal pausing),是转录延伸过程中重要的限速步骤和检查点[117]。不能继续延伸的Pol Ⅱ在INTAC (integrator-containing PP2A-AC)复合物的作用下,从启动子附近直接解离,提前终止转录[118]。INTAC复合物由两个模块组成,包括Integrator整合复合物和PP2A磷酸酶复合物。在INTAC介导的转录终止过程中,Integrator模块切割新生RNA的同时破坏活性中心中的RNA-DNA杂合双链,促进Pol Ⅱ从DNA上解离[119]。
4.3 Pol Ⅳ和Pol Ⅴ的特殊转录机制虽然Pol Ⅳ/Ⅴ由Pol Ⅱ进化而来,然而漫长的进化使Pol Ⅳ/Ⅴ的催化活性中心和外部结构单元与Pol Ⅱ具有显著区别。一方面,Pol Ⅳ/Ⅴ不与Pol Ⅱ的转录起始和延伸因子相互作用(如TFⅡB、TFⅡ E、TFⅡF和TFⅡS),从而保证Pol Ⅳ/Ⅴ和Pol Ⅱ转录互不干扰[120, 121];另一方面,Pol Ⅳ/Ⅴ催化中心的核心元件发生变化,导致Pol Ⅳ/Ⅴ的RNA延伸过程容易发生停滞和倒退[122-123]。
Pol Ⅳ和RDR2形成稳定的双RNA聚合酶复合物,在该复合物中两个RNA聚合酶的催化中心由一个内部的通道相连接。Pol Ⅳ首先被CLSYs、ZMP、SHH1、REM等蛋白以未知的机制招募到特定基因组区域,起始单链RNA的合成。Pol Ⅳ起始RNA合成之后,由于Pol Ⅳ具有较弱的RNA延伸能力,其转录过程容易发生暂停和倒退,在其倒退的过程中,单链RNA从Pol Ⅳ-RDR2的内部通道进入RDR2催化中心,作为模板开始第二条RNA的合成,RDR2在不断合成双链RNA的同时会诱导Pol Ⅳ进一步倒退,促使RNA从Pol Ⅳ催化中心完全转移到RDR2,最终RDR2完成双链RNA合成并将其释放[120, 122]。
Pol Ⅴ被DDR (DRD1-DMS3-RDM1)复合物招募到基因组特定区域起始转录。在转录延伸过程中,Pol Ⅴ与DNA和RNA能够形成特殊的相互作用,导致其转录易发生停顿和回溯。这种特殊的转录特征使Pol Ⅴ在转录延伸过程中,能够提供AGO4/6的结合时间窗口,从而进一步招募DRM2,在基因组特定位置上沉积甲基化修饰。目前关于Pol Ⅴ转录起始和转录偶联DNA甲基化的分子机制仍不清楚。
5 展望近年来,随着单颗粒冷冻电镜和单分子磁镊、单分子荧光等技术的发展,细菌、古菌、真核细胞RNA聚合酶的高分辨率三维结构已得到全面解析,然而转录过程中复杂中间状态的高分辨率三维结构尚未得到全面解析,上述过程的分子机制尚未阐明。细菌基因转录与DNA修复、蛋白质翻译等过程直接偶联,真核细胞Pol Ⅱ mRNA转录与内含子剪接、表观遗传修饰等过程直接偶联,上述过程的高分辨三维结构尚待全面解析。此外,细胞内基因转录过程的原位结构解析才初步开展,解析RNA聚合酶在细胞内的原位结构将揭示基因转录在生理状态下的工作机制和调控机制,未来冷冻电镜断层扫描技术的发展能够为基因转录的结构生物学研究带来新的突破。
致谢 感谢国家蛋白质科学研究(上海)设施在冷冻电镜样品制备、样品筛选和数据收集等方面提供的大力支持。感谢国家自然科学基金委杰出青年基金(32425006)、上海市基础研究特区计划(JCYJ-SHFY-2022-012)对相关研究的资助。| [1] |
Yang DL, Huang K, Deng D, et al. DNA-dependent RNA polymerases in plants. Plant Cell, 2023, 35: 3641-61. |
| [2] |
Girbig M, Misiaszek AD, Müller CW. Structural insights into nuclear transcription by eukaryotic DNA-dependent RNA polymerases. Nat Rev Mol Cell Biol, 2022, 23: 603-22. |
| [3] |
Xie G, Du X, Hu H, et al. Molecular mechanisms underlying the establishment, maintenance, and removal of DNA methylation in plants. Annu Rev Plant Biol, 2025, 76: 143-70. |
| [4] |
Flynn N, Chen X, Chen M. Plastid transcription: a major regulatory point in chloroplast biogenesis[M]//Burch-Smith TM. Chloroplast gene expression: regulation, stress signaling and biotechnology. Cham: Springer Nature Switzerland, 2024: 1-38
|
| [5] |
Wu XX, Mu WH, Li F, et al. Cryo-EM structures of the plant plastid-encoded RNA polymerase. Cell, 2024, 187: 1127-44. |
| [6] |
Chamberlin M, Berg P. Deoxyribonucleic acid-directed synthesis of ribonucleic acid by an enzyme from Escherichia coli. Proc Natl Acad Sci U S A, 1962, 48: 81-94. |
| [7] |
Zhang GY, Campbell EA, Minakhin L, et al. Crystal structure of core RNA polymerase at 3.3 Å resolution. Cell, 1999, 98: 811-24. |
| [8] |
Mazumder A, Kapanidis AN. Recent advances in understanding σ70-dependent transcription initiation mechanisms. J Mol Biol, 2019, 431: 3947-59. |
| [9] |
Lee DJ, Minchin SD, Busby SJ. Activating transcription in bacteria. Annu Rev Microbiol, 2012, 66: 125-52. |
| [10] |
Chen J, Boyaci H, Campbell EA. Diverse and unified mechanisms of transcription initiation in bacteria. Nat Rev Microbiol, 2021, 19: 95-109. |
| [11] |
Shen L, Lai G, You L, et al. An SI3-sigma arch stabilizes cyanobacteria transcription initiation complex. Proc Natl Acad Sci U S A, 2023, 120: e2219290120. |
| [12] |
Qayyum MZ, Imashimizu M, Leanca M, et al. Structure and function of the Si3 insertion integrated into the trigger loop/helix of cyanobacterial RNA polymerase. Proc Natl Acad Sci U S A, 2024, 121: e2311480121. |
| [13] |
Tewary A, Prajapati RK, Mukhopadhyay J. Mechanism of delta mediated transcription activation in Bacillus subtilis: interaction with α CTD of RNA polymerase stabilizes δ and successively facilitates the open complex formation. J Mol Biol, 2023, 435: 168366. |
| [14] |
Pei HH, Hilal T, Chen ZA, et al. The δ subunit and NTPase HelD institute a two-pronged mechanism for RNA polymerase recycling. Nat Commun, 2020, 11: 6418. |
| [15] |
Fang C, Li L, Zhao Y, et al. The bacterial multidrug resistance regulator BmrR distorts promoter DNA to activate transcription. Nat Commun, 2020, 11: 6284. |
| [16] |
Bock R. Witnessing genome evolution: experimental reconstruction of endosymbiotic and horizontal gene transfer. Annu Rev Genet, 2017, 51: 1-22. |
| [17] |
Daniell H, Jin S, Zhu XG, et al. Green giant--a tiny chloroplast genome with mighty power to produce high-value proteins: history and phylogeny. Plant Biotechnol J, 2021, 19: 430-47. |
| [18] |
Vergara-Cruces A, Pramanick I, Pearce D, et al. Structure of the plant plastid-encoded RNA polymerase. Cell, 2024, 187: 1145-59.e21. |
| [19] |
Wang T, Wang GL, Fang Y, et al. Architecture of the spinach plastid-encoded RNA polymerase. Nat Commun, 2024, 15: 9838. |
| [20] |
do Prado PFV, Ahrens FM, Liebers M, et al. Structure of the multi-subunit chloroplast RNA polymerase. Mol Cell, 2024, 84: 910-25.e5. |
| [21] |
Jun SH, Hyun J, Cha JS, et al. Direct binding of TFEα opens DNA binding cleft of RNA polymerase. Nat Commun, 2020, 11: 6123. |
| [22] |
Blombach F, Matelska D, Fouqueau T, et al. Key concepts and challenges in archaeal transcription. J Mol Biol, 2019, 431: 4184-201. |
| [23] |
Pilotto S, Fouqueau T, Lukoyanova N, et al. Structural basis of RNA polymerase inhibition by viral and host factors. Nat Commun, 2021, 12: 5523. |
| [24] |
Tarau D, Grunberger F, Pilsl M, et al. Structural basis of archaeal RNA polymerase transcription elongation and Spt4/5 recruitment. Nucleic Acids Res, 2024, 52: 6017-35. |
| [25] |
Werner F, Grohmann D. Evolution of multisubunit RNA polymerases in the three domains of life. Nat Rev Microbiol, 2011, 9: 85-98. |
| [26] |
Cramer P. Organization and regulation of gene transcription. Nature, 2019, 573: 45-54. |
| [27] |
Vannini A, Cramer P. Conservation between the RNA polymerase Ⅰ, Ⅱ, and Ⅲ transcription initiation machineries. Mol Cell, 2012, 45: 439-46. |
| [28] |
Chedin S, Riva M, Schultz P, et al. The RNA cleavage activity of RNA polymerase Ⅲ is mediated by an essential TFⅡS-like subunit and is important for transcription termination. Genes Dev, 1998, 12: 3857-71. |
| [29] |
Werner M, Thuriaux P, Soutourina J. Structure-function analysis of RNA polymerases Ⅰ and Ⅲ. Curr Opin Struct Biol, 2009, 19: 740-5. |
| [30] |
Kuhn CD, Geiger SR, Baumli S, et al. Functional architecture of RNA polymerase Ⅰ. Cell, 2007, 131: 1260-72. |
| [31] |
Kim YJ, Björklund S, Li Y, et al. A multiprotein mediator of transcriptional activation and its interaction with the C-terminal repeat domain of RNA polymerase Ⅱ. Cell, 1994, 77: 599-608. |
| [32] |
Hsin JP, Manley JL. The RNA polymerase Ⅱ CTD coordinates transcription and RNA processing. Genes Dev, 2012, 26: 2119-37. |
| [33] |
Zaborowska J, Egloff S, Murphy S. The pol Ⅱ CTD: new twists in the tail. Nat Struct Mol Biol, 2016, 23: 771-7. |
| [34] |
Jeronimo C, Collin P, Robert F. The RNA polymerase Ⅱ CTD: the increasing complexity of a low-complexity protein domain. J Mol Biol, 2016, 428: 2607-22. |
| [35] |
Carter R, Drouin G. The increase in the number of subunits in eukaryotic RNA polymerase Ⅲ relative to RNA polymerase Ⅱ is due to the permanent recruitment of general transcription factors. Mol Biol Evol, 2010, 27: 1035-43. |
| [36] |
Geiger SR, Lorenzen K, Schreieck A, et al. RNA polymerase Ⅰ contains a TFⅡF-related DNA-binding subcomplex. Mol Cell, 2010, 39: 583-94. |
| [37] |
The Arabidopsis Genome Initiative. Analysis of the genome sequence of the flowering plant Arabidopsis thaliana. Nature, 2000, 408: 796-815. |
| [38] |
Dubin MJ, Mittelsten Scheid O, Becker C. Transposons: a blessing curse. Curr Opin Plant Biol, 2018, 42: 23-9. |
| [39] |
Matzke MA, Mosher RA. RNA-directed DNA methylation: an epigenetic pathway of increasing complexity. Nat Rev Genet, 2014, 15: 394-408. |
| [40] |
Huang L, Jones AM, Searle I, et al. An atypical RNA polymerase involved in RNA silencing shares small subunits with RNA polymerase Ⅱ. Nat Struct Mol Biol, 2009, 16: 91-3. |
| [41] |
Haag JR, Pikaard CS. Multisubunit RNA polymerases Ⅳ and Ⅴ: purveyors of non-coding RNA for plant gene silencing. Nat Rev Mol Cell Biol, 2011, 12: 483-92. |
| [42] |
Luo J, Hall BD. A multistep process gave rise to RNA polymerase Ⅳ of land plants. J Mol Evol, 2007, 64: 101-12. |
| [43] |
Ream TS, Haag JR, Wierzbicki AT, et al. Subunit compositions of the RNA-silencing enzymes Pol Ⅳ and Pol Ⅴ reveal their origins as specialized forms of RNA polymerase Ⅱ. Mol Cell, 2009, 33: 192-203. |
| [44] |
Tucker SL, Reece J, Ream TS, et al. Evolutionary history of plant multisubunit RNA polymerases Ⅳ and Ⅴ: subunit origins via genome-wide and segmental gene duplications, retrotransposition, and lineage-specific subfunctionalization. Cold Spring Harb Symp Quant Biol, 2010, 75: 285-97. |
| [45] |
Wang SB, Liang HP, Xu Y, et al. Genome-wide analyses across Viridiplantae reveal the origin and diversification of small RNA pathway-related genes. Commun Biol, 2021, 4: 412. |
| [46] |
Feklistov A, Sharon BD, Darst SA, et al. Bacterial sigma factors: a historical, structural, and genomic perspective. Annu Rev Microbiol, 2014, 68: 357-76. |
| [47] |
Mascher T. Signaling diversity and evolution of extracytoplasmic function (ECF) sigma factors. Curr Opin Microbiol, 2013, 16: 148-55. |
| [48] |
Campbell EA, Kamath S, Rajashankar KR, et al. Crystal structure of Aquifex aeolicus σN bound to promoter DNA and the structure of σN-holoenzyme. Proc Natl Acad Sci U S A, 2017, 114: E1805-E14. |
| [49] |
Danson AE, Jovanovic M, Buck M, et al. Mechanisms of σ-dependent transcription initiation and regulation. J Mol Biol, 2019, 431: 3960-74. |
| [50] |
Saecker RM, Mueller AU, Malone B, et al. Early intermediates in bacterial RNA polymerase promoter melting visualized by time-resolved cryo-electron microscopy. Nat Struct Mol Biol, 2024, 31: 1778-88. |
| [51] |
Chen J, Chiu C, Gopalkrishnan S, et al. Stepwise promoter melting by bacterial RNA polymerase. Mol Cell, 2020, 78: 275-88. |
| [52] |
Zuo Y, Steitz TA. Crystal structures of the E. coli transcription initiation complexes with a complete bubble. Mol Cell, 2015, 58: 534-40. |
| [53] |
Zhang Y, Feng Y, Chatterjee S, et al. Structural basis of transcription initiation. Science, 2012, 338: 1076-80. |
| [54] |
Li L, Molodtsov V, Lin W, et al. RNA extension drives a stepwise displacement of an initiation-factor structural module in initial transcription. Proc Natl Acad Sci U S A, 2020, 117: 5801-9. |
| [55] |
Kapanidis AN, Margeat E, Ho SO, et al. Initial transcription by RNA polymerase proceeds through a DNA-scrunching mechanism. Science, 2006, 314: 1144-7. |
| [56] |
Li L, Fang C, Zhuang N, et al. Structural basis for transcription initiation by bacterial ECF sigma factors. Nat Commun, 2019, 10: 1153. |
| [57] |
Lin W, Mandal S, Degen D, et al. Structural basis of ECF-sigma-factor-dependent transcription initiation. Nat Commun, 2019, 10: 710. |
| [58] |
Fang C, Li L, Shen L, et al. Structures and mechanism of transcription initiation by bacterial ECF factors. Nucleic Acids Res, 2019, 47: 7094-104. |
| [59] |
Yang Y, Darbari VC, Zhang N, et al. Structures of the RNA polymerase-σ54 reveal new and conserved regulatory strategies. Science, 2015, 349: 882-5. DOI:10.1126/science.aab1478 |
| [60] |
Gao F, Ye F, Buck M, et al. Subunit specialization in AAA+ proteins and substrate unfolding during transcription complex remodeling. Proc Natl Acad Sci U S A, 2025, 122: e2425868122. |
| [61] |
Ye F, Gao F, Liu X, et al. Mechanisms of DNA opening revealed in AAA+ transcription complex structures. Sci Adv, 2022, 8: eadd3479. |
| [62] |
Madan Babu M, Teichmann SA. Evolution of transcription factors and the gene regulatory network in Escherichia coli. Nucleic Acids Res, 2003, 31: 1234-44. |
| [63] |
Busby S, Ebright RH. Transcription activation by catabolite activator protein (CAP). J Mol Biol, 1999, 293: 199-213. |
| [64] |
Lawson CL, Swigon D, Murakami KS, et al. Catabolite activator protein: DNA binding and transcription activation. Curr Opin Struct Biol, 2004, 14: 10-20. |
| [65] |
Kompaniiets D, Wang D, Yang Y, et al. Structure and molecular mechanism of bacterial transcription activation. Trends Microbiol, 2024, 32: 379-97. |
| [66] |
Liu B, Hong C, Huang RK, et al. Structural basis of bacterial transcription activation. Science, 2017, 358: 947-51. |
| [67] |
Feng Y, Zhang Y, Ebright RH. Structural basis of transcription activation. Science, 2016, 352: 1330-3. |
| [68] |
Fang CL, Philips SJ, Wu XX, et al. CueR activates transcription through a DNA distortion mechanism. Nat Chem Biol, 2021, 17: 57-64. |
| [69] |
Fang CL, Zhang Y. Bacterial MerR family transcription regulators: activation by distortion. Acta Biochim Biophys Sin, 2022, 54: 25-36. |
| [70] |
Yang Y, Liu C, Zhou W, et al. Structural visualization of transcription activated by a multidrug-sensing MerR family regulator. Nat Commun, 2021, 12: 2702. |
| [71] |
He D, You L, Wu X, et al. Pseudomonas aeruginosa SutA wedges RNAP lobe domain open to facilitate promoter DNA unwinding. Nat Commun, 2022, 13: 4204. |
| [72] |
Ray-Soni A, Bellecourt MJ, Landick R. Mechanisms of bacterial transcription termination: all good things must end. Annu Rev Biochem, 2016, 85: 319-47. |
| [73] |
Roberts JW. Mechanisms of bacterial transcription termination. J Mol Biol, 2019, 431: 4030-9. |
| [74] |
Mitra P, Ghosh G, Hafeezunnisa M, et al. Rho protein: roles and mechanisms. Annu Rev Microbiol, 2017, 71: 687-709. |
| [75] |
Shi J, Wen A, Zhao M, et al. Structural basis of Mfd-dependent transcription termination. Nucleic Acids Res, 2020, 48: 11762-72. |
| [76] |
Kang JY, Llewellyn E, Chen J, et al. Structural basis for transcription complex disruption by the Mfd translocase. Elife, 2021, 10: e62117. |
| [77] |
Wang L, Watters JW, Ju XW, et al. Head-on and co-directional RNA polymerase collisions orchestrate bidirectional transcription termination. Mol Cell, 2023, 83: 1153-64. |
| [78] |
You L, Zhang, Y. Progress on molecular mechanisms of bacterial transcription termination. Hereditas, 2024, 46: 982-94. |
| [79] |
Peters JM, Mooney RA, Kuan PF, et al. Rho directs widespread termination of intragenic and stable RNA transcription. Proc Natl Acad Sci U S A, 2009, 106: 15406-11. |
| [80] |
Gusarov I, Nudler E. The mechanism of intrinsic transcription termination. Mol Cell, 1999, 3: 495-504. |
| [81] |
Yarnell WS, Roberts JW. Mechanism of intrinsic transcription termination and antitermination. Science, 1999, 284: 611-5. |
| [82] |
You L, Omollo EO, Yu C, et al. Structural basis for intrinsic transcription termination. Nature, 2023, 613: 783-9. |
| [83] |
Kang W, Ha KS, Uhm H, et al. Transcription reinitiation by recycling RNA polymerase that diffuses on DNA after releasing terminated RNA. Nat Commun, 2020, 11: 450. |
| [84] |
Harden TT, Herlambang KS, Chamberlain M, et al. Alternative transcription cycle for bacterial RNA polymerase. Nat Commun, 2020, 11: 448. |
| [85] |
Geiselmann J, Yager TD, Gill SC, et al. Physical properties of the Escherichia coli transcription termination factor rho. 1. Association states and geometry of the rho hexamer. Biochemistry, 1992, 31: 111-21. |
| [86] |
Molodtsov V, Wang CY, Firlar E, et al. Structural basis of Rho-dependent transcription termination. Nature, 2023, 614: 367-74. |
| [87] |
Skordalakes E, Berger JM. Structure of the Rho transcription terminator: mechanism of mRNA recognition and helicase loading. Cell, 2003, 114: 135-46. |
| [88] |
Song E, Uhm H, Munasingha PR, et al. Rho-dependent transcription termination proceeds via three routes. Nat Commun, 2022, 13: 1663. |
| [89] |
Said N, Hilal T, Sunday ND, et al. Steps toward translocation-independent RNA polymerase inactivation by terminator ATPase ρ. Science, 2021, 371: eabd1673. |
| [90] |
Hao Z, Epshtein V, Kim KH, et al. Pre-termination transcription complex: structure and function. Mol Cell, 2021, 81: 281-92. |
| [91] |
Nechaev S, Severinov K. Bacteriophage-induced modifications of host RNA polymerase. Annu Rev Microbiol, 2003, 57: 301-22. |
| [92] |
Krupp F, Said N, Huang YH, et al. Structural basis for the action of an all-purpose transcription anti-termination factor. Mol Cell, 2019, 74: 143-57. |
| [93] |
Shi J, Gao X, Tian T, et al. Structural basis of Q-dependent transcription antitermination. Nat Commun, 2019, 10: 2925. |
| [94] |
Yin Z, Kaelber JT, Ebright RH. Structural basis of Q-dependent antitermination. Proc Natl Acad Sci U S A, 2019, 116: 18384-90. |
| [95] |
Nechaev S, Yuzenkova Y, Niedziela-Majka A, et al. A novel bacteriophage-encoded RNA polymerase binding protein inhibits transcription initiation and abolishes transcription termination by host RNA polymerase. J Mol Biol, 2002, 320: 11-22. |
| [96] |
You LL, Shi J, Shen LQ, et al. Structural basis for transcription antitermination at bacterial intrinsic terminator. Nat Commun, 2019, 10: 3048. |
| [97] |
Fouqueau T, Blombach F, Cackett G, et al. The cutting edge of archaeal transcription. Emerg Top Life Sci, 2018, 2: 517-33. |
| [98] |
Gehring AM, Walker JE, Santangelo TJ. Transcription regulation in Archaea. J Bacteriol, 2016, 198: 1906-17. DOI:10.1128/jb.00255-16 |
| [99] |
Li J, Yue L, Li Z, et al. aCPSF1 cooperates with terminator U-tract to dictate archaeal transcription termination efficacy. Elife, 2021, 10: e70464. |
| [100] |
Sanders TJ, Wenck BR, Selan JN, et al. FttA is a CPSF73 homologue that terminates transcription in Archaea. Nat Microbiol, 2020, 5: 545-53. |
| [101] |
Yue L, Li J, Zhang B, et al. The conserved ribonuclease aCPSF1 triggers genome-wide transcription termination of Archaea via a 3′-end cleavage mode. Nucleic Acids Res, 2020, 48: 9589-605. |
| [102] |
You L, Wang C, Molodtsov V, et al. Structural basis of archaeal FttA-dependent transcription termination. Nature, 2024, 635: 229-36. |
| [103] |
Ji D, Manavski N, Meurer J, et al. Regulated chloroplast transcription termination. Biochim Biophys Acta Bioenerg, 2019, 1860: 69-77. |
| [104] |
Chi W, He B, Manavski N, et al. RHON1 mediates a Rho-like activity for transcription termination in plastids of Arabidopsis thaliana. Plant Cell, 2014, 26: 4918-32. |
| [105] |
Chen X, Qi Y, Wu Z, et al. Structural insights into preinitiation complex assembly on core promoters. Science, 2021, 372: eaba8490. DOI:10.1126/science.aba8490 |
| [106] |
Chen X, Wang X, Liu W, et al. Structures of +1 nucleosome- bound PIC-Mediator complex. Science, 2022, 378: 62-8. |
| [107] |
Chen X, Liu W, Wang Q, et al. Structural visualization of transcription initiation in action. Science, 2023, 382: eadi5120. DOI:10.1126/science.adi5120 |
| [108] |
Chen X, Yin X, Li J, et al. Structures of the human Mediator and Mediator-bound preinitiation complex. Science, 2021, 372: eabg0635. |
| [109] |
Thomas MC, Chiang CM. The general transcription machinery and general cofactors. Crit Rev Biochem Mol Biol, 2006, 41: 105-78. |
| [110] |
Glover-Cutter K, Larochelle S, Erickson B, et al. TFⅡH-associated Cdk7 kinase functions in phosphorylation of C-terminal domain Ser7 residues, promoter-proximal pausing, and termination by RNA polymerase Ⅱ. Mol Cell Biol, 2009, 29: 5455-64. |
| [111] |
Porrua O, Libri D. Transcription termination and the control of the transcriptome: why, where and how to stop. Nat Rev Mol Cell Biol, 2015, 16: 190-202. |
| [112] |
Richard P, Manley JL. Transcription termination by nuclear RNA polymerases. Genes Dev, 2009, 23: 1247-69. |
| [113] |
Kim M, Vasiljeva L, Rando OJ, et al. Distinct pathways for snoRNA and mRNA termination. Mol Cell, 2006, 24: 723-34. |
| [114] |
Luo W, Johnson AW, Bentley DL. The role of Rat1 in coupling mRNA 3′-end processing to transcription termination: implications for a unified allosteric-torpedo model. Genes Dev, 2006, 20: 954-65. |
| [115] |
Chaves-Arquero B, Perez-Canadillas JM. The Nrd1-Nab3-Sen1 transcription termination complex from a structural perspective. Biochem Soc Trans, 2023, 51: 1257-69. |
| [116] |
Rengachari S, Hainthaler T, Oberthuer C, et al. Mechanism of polyadenylation-independent RNA polymerase Ⅱ termination. Nat Struct Mol Biol, 2025, 32: 339-45. |
| [117] |
Dollinger R, Gilmour DS. Regulation of promoter proximal pausing of RNA polymerase Ⅱ in Metazoans. J Mol Biol, 2021, 433: 166897. |
| [118] |
Fianu I, Chen Y, Dienemann C, et al. Structural basis of Integrator-mediated transcription regulation. Science, 2021, 374: 883-7. |
| [119] |
Fianu I, Ochmann M, Walshe JL, et al. Structural basis of Integrator-dependent RNA polymerase Ⅱ termination. Nature, 2024, 629: 219-27. |
| [120] |
Huang K, Wu XX, Fang CL, et al. Pol Ⅳ and RDR2: a two-RNA-polymerase machine that produces double-stranded RNA. Science, 2021, 374: 1579-86. DOI:10.1126/science.abj9184 |
| [121] |
Zhang HW, Huang K, Gu ZX, et al. A cryo-EM structure of KTF1-bound polymerase Ⅴ transcription elongation complex. Nat Commun, 2023, 14: 3118. |
| [122] |
Fang C, Huang K, Wu X, et al. Transcription elongation of the plant RNA polymerase Ⅳ is prone to backtracking. Sci Adv, 2024, 10: eadq3087. DOI:10.1126/sciadv.adq3087 |
| [123] |
Xie G, Du X, Hu H, et al. Structure and mechanism of the plant RNA polymerase Ⅴ. Science, 2023, 379: 1209-13. |
 2025, Vol. 37
2025, Vol. 37 

 张余,中国科学院分子植物科学卓越创新中心研究员。2004年毕业于复旦大学,获学士学位;2009年毕业于中国科学院上海药物研究所,获博士学位;2009—2015年,在美国罗格斯大学从事博士后研究;2015年8月起在现单位担任研究员。张余博士从结构生物学角度出发,探索基因转录的工作机制和调控机制,率领团队解析了mRNA的转录终止机制,提出多种细菌转录调控模型,解析了植物功能特化的RNA聚合酶的结构和工作机制。研究成果以通讯作者(含共同)在Cell、Science、Nature等杂志发表论文20余篇
张余,中国科学院分子植物科学卓越创新中心研究员。2004年毕业于复旦大学,获学士学位;2009年毕业于中国科学院上海药物研究所,获博士学位;2009—2015年,在美国罗格斯大学从事博士后研究;2015年8月起在现单位担任研究员。张余博士从结构生物学角度出发,探索基因转录的工作机制和调控机制,率领团队解析了mRNA的转录终止机制,提出多种细菌转录调控模型,解析了植物功能特化的RNA聚合酶的结构和工作机制。研究成果以通讯作者(含共同)在Cell、Science、Nature等杂志发表论文20余篇